

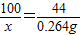
 =0.24g=240mg
=0.24g=240mg

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
 某种补钙剂的产品说明书如下表:某同学要探究该钙片的主要成分中碳酸钙的含量是否准确,他取出l0片钙片,加入足量的稀盐酸,充分反应,收集到2.64g二氧化碳(假定其它成分不与盐酸反应).试计算:
某种补钙剂的产品说明书如下表:某同学要探究该钙片的主要成分中碳酸钙的含量是否准确,他取出l0片钙片,加入足量的稀盐酸,充分反应,收集到2.64g二氧化碳(假定其它成分不与盐酸反应).试计算:查看答案和解析>>
科目:初中化学 来源: 题型:
 (2010?怀化)钙是维持人体正常功能所必需的元素,如图所示为某种补钙剂“钙尔奇“说明书的一部分.某校化学兴趣小组为测定“钙尔奇”中碳酸钙的含量,做了如下实验:取2片“钙尔奇“研成粉末,全部倒入一烧杯中,再往烧杯中滴加稀盐酸,直到刚好不再产生气泡时停止滴加稀盐酸,刚好用去稀盐酸30克,生成了二氧化碳1.32g.
(2010?怀化)钙是维持人体正常功能所必需的元素,如图所示为某种补钙剂“钙尔奇“说明书的一部分.某校化学兴趣小组为测定“钙尔奇”中碳酸钙的含量,做了如下实验:取2片“钙尔奇“研成粉末,全部倒入一烧杯中,再往烧杯中滴加稀盐酸,直到刚好不再产生气泡时停止滴加稀盐酸,刚好用去稀盐酸30克,生成了二氧化碳1.32g.查看答案和解析>>
科目:初中化学 来源: 题型:
| 加入稀盐酸的质量/g | 剩余固体的质量/g | |
| 第一次 | 10.0 | 7.0 |
| 第二次 | 10.0 | m |
| 第三次 | 10.0 | 2.0 |
| 第四次 | 10.0 | n |

| 反应前 | 烧杯+1片钙尔奇+稀盐酸 | 32.00g |
| 反应后 | 烧杯+烧杯内的物质 | 31.34g |
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com