
分析 镁和稀硫酸反应生成硫酸镁和氢气,根据氢气质量可以计算镁的质量和生成的硫酸镁的质量,进一步可以计算金属镁样品中杂质的质量和反应后所得溶液的溶质质量分数.
解答 解:(1)设镁的质量为x,生成硫酸镁质量为y,
Mg+H2SO4═MgSO4+H2↑,
24 120 2
x y 0.4g
$\frac{24}{x}$=$\frac{120}{y}$=$\frac{2}{0.4g}$,
x=4.8g,y=24g,
金属镁样品中杂质的质量为:5.0g-4.8g=0.2g,
故填:0.2.
(2)反应后所得溶液的溶质质量分数为:$\frac{24g}{4.8g+95.6g-0.4g}$×100%=24%,
答:反应后所得溶液的溶质质量分数为24%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:初中化学 来源: 题型:解答题

| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 实验操作 | 实验现象及结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D | |
| 实验 操作 | 把燃着的木条插入某瓶无色气体中 | 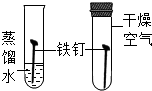 | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 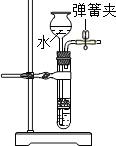 |
| 现象 | 木条熄灭 | 放置一周后,A中铁钉生锈,B中铁钉无明显变化 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 放置一段时间,长颈漏斗中水面下降 |
| 结论 | 瓶中的气体是二氧化碳 | 铁生锈需要氧气和水 | 氧气是燃烧需要的条件之一 | 装置气密性良好 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 水是生命之源,通过化学学习,我们进一步认识到水的重要作用.
水是生命之源,通过化学学习,我们进一步认识到水的重要作用.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 编号 | 1 | 2 | 3 | 4 |
| 加入水的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 7.25 | 4.05 | 3 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某实验小组的同学设计了如下实验探究可燃物燃烧的条件:
某实验小组的同学设计了如下实验探究可燃物燃烧的条件:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com