
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,用pH试纸检测滤液的pH | ①生成白色沉淀 ②pH>7 | 猜想③正确 |
分析 (1)根据氧化钙能与水化合生成氢氧化钙放出了大量的热、氢氧化钠溶于水时能够放出大量的热;
(2)过滤可以把不溶于水的物质和溶液分离,碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳;
(3)【猜想假设】根据氧化钙和氢氧化钠的性质对溶液B中的溶质;
【实验验证】根据氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,加入足量CaCl2溶液这样会除掉全部的碳酸钠.
解答 解:(1)由于氧化钙能与水化合生成氢氧化钙放出了大量的热、氢氧化钠溶于水时能够放出大量的热,所以样品中至少有氢氧化钠、氧化钙中的一种.分析选择项,D正确;
故填:D.
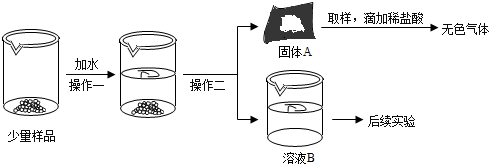
(2)操作二的名称是过滤,可以把形成的沉淀和溶液分离;氧化钙变质后能够形成的碳酸盐是碳酸钙,氢氧化钠变质后能够形成的碳酸盐是碳酸钠,两种物质和稀盐酸反应都能够生成二氧化碳,但是碳酸钠易溶于水,所以固体A中一定含有碳酸钙.
故填:碳酸钙.
(3)溶液B中溶质可能为:氢氧化钠,或碳酸钠,或氢氧化钠和碳酸钠,或氢氧化钙和氢氧化钠.
所以猜想三是:猜想四:Ca(OH)2和 NaOH.
①取少量溶液B于试管中,加入足量CaCl2溶液,产生了白色沉淀,说明溶液中含有碳酸钠;
②过滤,用pH试纸检测滤液的pH,由pH>7,说明溶液中含有氢氧化钠.
综合以上分析可知,猜想③正确.
由以上分析可知,实验步骤①中发生的化学方程式是:CaCl2+Na2CO3=2NaCl+CaCO3↓,其实验目的是 除尽溶液B中的Na2CO3,避免干扰NaOH的检验.
故填:NaOH;生成白色沉淀;CaCl2+Na2CO3=2NaCl+CaCO3↓;除尽溶液B中的Na2CO3,避免干扰NaOH的检验.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.所以,对化学实验不仅要认真观察,还应掌握设计实验、观察实验现象的方法.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:初中化学 来源: 题型:计算题
 实验室一瓶浓硫酸的商标如图所示,根据有关数据计算.
实验室一瓶浓硫酸的商标如图所示,根据有关数据计算.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2 | B. | H2O | C. | HNO3 | D. | H2O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中有气泡放出, 带火星的木条复燃. | 溶液中有气泡放出, | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com