
分析 根据铝和氧气反应生成氧化铝,以及反应基本类型进行解答;
根据铝和硫酸铜反应生成硫酸铝和铜,硫酸铝【Al2(SO4)3】和氟化钠(NaF)在共熔条件下反应生成冰晶石(Na3AlF6),同时得到硫酸钠【Na2SO4】进行分析.
解答 解:铝和氧气反应生成氧化铝,化学方程式为:4Al+3O2=2Al2O3,该反应满足化合反应多变一的条件,属于化合反应,铝和硫酸铜反应生成硫酸铝和铜,化学方程式为:2Al+3CuSO4=3Cu+Al2(SO4)3,硫酸铝和氟化钠在共熔条件下反应生成冰晶石和硫酸钠,化学方程式为:Al2(SO4)3+12NaF=2Na3AlF6+3Na2SO4.
故答案为:4Al+3O2=2Al2O3,化合,2Al+3CuSO4=3Cu+Al2(SO4)3,Al2(SO4)3+12NaF=2Na3AlF6+3Na2SO4.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 葡萄糖酸锌中锌元素的质量分数为31.6% | |
| B. | 葡萄糖酸锌不是氧化物 | |
| C. | 葡萄糖酸锌中碳、氢元素质量比为6:11 | |
| D. | 葡萄糖酸锌是由12个碳原子、22个氢原子、14个氧原子和1个锌原子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
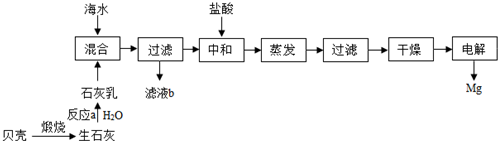
 1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:
1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气能被压缩--分子体积可以变小 | |
| B. | 湿衣服在充足的阳光下容易晾干--分子的运动速率随温度升高而加快 | |
| C. | 结冰的水不能流动--0℃以下,水分子不再运动 | |
| D. | 50mL水和50mL酒精混合后的总体积小于100mL--分子的质量和体积都很小 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaCl,K2SO4 | B. | H2SO4,CuSO4 | C. | NaNO3,NH4NO3 | D. | CaCl2,Na2CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com