
A.①②⑥ B.①②⑤ C.①③⑥ D.①④⑥
| 分析:这是一道根据一定质量的物质在氧气中完全燃烧,生成一定质量的若干产物,推断物质组成元素的题目.解题思路是:根据物质在发生化学反应前后元素种类不变,各元素总质量守恒的原则解题.由于参加反应的该物质质量确定,且只在氧气中反应,而生成的各种产物的名称质量也确定.因此,通过计算可以确定该种物质的组成元素及各元素的质量,进而确定各元素的原子个数比.
(1)由于生成物中只有二氧化碳和水,所以,参加反应的元素只有三种:C、H、O.其中C、H一定来源于该物质,O可能是氧气中的,也可能是氧气与该物质共有的. (2)通过计算可知:4.4 g二氧化碳中,含碳的质量是:4.4
g×碳元素的质量分数=4.4 g× (3)该物质中C、H两元素的原子个数比为:
|


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:初中化学 来源: 题型:058
某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质以后,联想到家庭中蒸制馒头
时常用的物质小苏打(NaHCO3),于是采用市售小苏打样品进行了如下的实验探究。
实验一: 探究碳酸氢钠的化学性质
(1)取样品溶于适量的水中,测得溶液的pH大于7。
(2)向小苏打固体中滴加盐酸,有大量气泡产生,该气体经检验是二氧化碳。
该反应的化学方程式为 。
(3)取小苏打的溶液加入澄清石灰水,生成了白色沉淀。
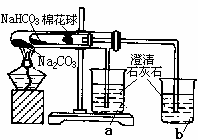
(4)同学们通过查阅资料,在老师的指导下采用了右图装置
对小苏打和纯碱做了对比实验。实验中小试管内沾有无水硫酸铜粉末的棉花球变成蓝色,a烧杯中石灰水无明显现象,
b
烧杯中石灰水出现白色浑浊。①在实验结束时,操作上要特别注意的问题是:
;
②由实验现象可以得出的结论是 。
(5)请你根据以上实验,归纳出小苏打的化学性质(至少三点):
。
实验二: 测定小苏打样品中NaHCO3的质量分数
市售的小苏打样品NaHCO3的质量分数的标注为95%,该兴趣小组对此产生了疑问,于是又进行了下面的实验。(假设小苏打样品中的杂质可溶解于水,对实验测定无影响)
方案1:取10 g固体样品加水完全溶解后,加入足量澄清石灰水,反应方程式如下:
Ca(OH)2 + NaHCO3= CaCO3
↓+ NaOH + H2O ,过滤得到沉淀CaCO3, 干燥后称量质量为10 g。经计算得到NaHCO3质量为8.4g。结论:小苏打样品中NaHCO3的质量分数仅为84 %,低于标注。
利用本题中给出的信息,请你设计出新的测定方案,简述实验方法和结论。
(6)方案2:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
根据题意填写下列空格:
(1)某微粒的结构示意图为 ![]() ,若X等于11,则该微粒表示_____???___(填“阳”
,若X等于11,则该微粒表示_____???___(填“阳”
或“阴”)离子。在N、N2、2N2三种符号中,只表示微观意义,而不表示宏观意义的是
(2)构成物质的基本微粒有分子、原子、离子。氯化钠是由 构成的;水是由 构成的;金(Au)是由 构成的。
(3)有下列物质:CO2 、CO 、H2 、CH4 ,其中通入紫色石蕊溶液,溶液变红的是___________, 最理想的燃料是_____???_____,属于有机物的是_____???_____。
(4)加钙牛奶中的“钙”是指 (填“元素”或“原子”),身体中一旦缺钙,可能患
有的疾病是 (填“骨质疏松”或“贫血”)。
(5)通过晾晒海水或煮盐井水、盐湖水等方法,均可得到含有较多杂质的粗盐,这种方
法属于__________变化(填“物理”或“化学”)。粗盐经过__________、过滤、__________
可得到初步提纯,再通过化学方法获得精盐。
(6)某同学用提取的精盐配制100g质量分数为11.7%的氯化钠溶液,请你参与完成:
①计算:氯化钠的质量为 g,水为 g。
②称量:用托盘天平称量,氯化钠应放在 (填“左盘”或“右盘”)。
③溶解:用量筒来量取所需的水(水的密度为1g/cm3),量筒的规格是 (从下列中选用:10mL、25 mL、50 mL、100 mL)。量取液体时,量筒必须放平,视线与液体的_________ 保持水平。溶解氯化钠要用到玻璃棒,其作用是 。
④反思:若称取的氯化钠中含有水分,则所配制的溶液溶质质量分数会 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
根据题意填写下列空格:
(1)某微粒的结构示意图为 ![]() ,若X等于11,则该微粒表示_____???___(填“阳”或“阴”)离子。在N、N2、2N2三种符号中,只表示微观意义,而不表示宏观意义的是
,若X等于11,则该微粒表示_____???___(填“阳”或“阴”)离子。在N、N2、2N2三种符号中,只表示微观意义,而不表示宏观意义的是
(2)构成物质的基本微粒有分子、原子、离子。氯化钠是由 构成的;水是由 构成的;金(Au)是由 构成的。
(3)有下列物质:CO2 、CO 、H2 、CH4 ,其中通入紫色石蕊溶液,溶液变红的是___________, 最理想的燃料是_____???_____,属于有机物的是_____???_____。
(4)加钙牛奶中的“钙”是指 (填“元素”或“原子”),身体中一旦缺钙,可能患有的疾病是 (填“骨质疏松”或“贫血”)。
(5)通过晾晒海水或煮盐井水、盐湖水等方法,均可得到含有较多杂质的粗盐,这种方法属于__________变化(填“物理”或“化学”)。粗盐经过__________、过滤、__________
可得到初步提纯,再通过化学方法获得精盐。
(6)某同学用提取的精盐配制100g质量分数为11.7%的氯化钠溶液,请你参与完成:
①计算:氯化钠的质量为 g,水为 g。
②称量:用托盘天平称量,氯化钠应放在 (填“左盘”或“右盘”)。
③溶解:用量筒来量取所需的水(水的密度为1g/cm3),量筒的规格是 (从下列中选用:10mL、25 mL、50 mL、100 mL)。量取液体时,量筒必须放平,视线与液体的_________ 保持水平。溶解氯化钠要用到玻璃棒,其作用是 。
④反思:若称取的氯化钠中含有水分,则所配制的溶液溶质质量分数会 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
根据题意填写下列空格:
(1)某微粒的结构示意图为![]() ,若X等于11,则该微粒表示_____???___(填“阳”
,若X等于11,则该微粒表示_____???___(填“阳”
或“阴”)离子。在N、N2、2N2三种符号中,只表示微观意义,而不表示宏观意义的是
(2)构成物质的基本微粒有分子、原子、离子。氯化钠是由 构成的;水是由 构成的;金(Au)是由 构成的。
(3)有下列物质:CO2 、CO 、H2 、CH4 ,其中通入紫色石蕊溶液,溶液变红的是___________, 最理想的燃料是_____???_____,属于有机物的是_____???_____。
(4)加钙牛奶中的“钙”是指 (填“元素”或“原子”),身体中一旦缺钙,可能患有的疾病是 (填“骨质疏松”或“贫血”)。
(5)通过晾晒海水或煮盐井水、盐湖水等方法,均可得到含有较多杂质的粗盐,这种方
法属于__________变化(填“物理”或“化学”)。粗盐经过__________、过滤、__________
可得到初步提纯,再通过化学方法获得精盐。
(6)某同学用提取的精盐配制100g质量分数为11.7%的氯化钠溶液,请你参与完成:
①计算:氯化钠的质量为 g,水为 g。
②称量:用托盘天平称量,氯化钠应放在 (填“左盘”或“右盘”)。
③溶解:用量筒来量取所需的水(水的密度为1g/cm3),量筒的规格是 (从下列中选用:10mL、25 mL、50 mL、100 mL)。量取液体时,量筒必须放平,视线与液体的_________ 保持水平。溶解氯化钠要用到玻璃棒,其作用是 。
④反思:若称取的氯化钠中含有水分,则所配制的溶液溶质质量分数会 (填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com