
【题目】水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)“生命吸管”(如右图)是一种可以随身携带的小型水净化器,里面装有网丝、注入了活性炭和碘的树脂等。其中活性炭起到________和过滤的作用。
(2)水常用来配制各种溶液,硝酸钾溶液中的溶质为________。
(3)农业生产常用溶质的质量分数为10% ~ 20%的NaCl溶液来选种。现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为________g。
(4)根据下表回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度 | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
①60 ℃时,向两个分别盛有50 g NaCl和NH4Cl的烧杯中,各加入100 g的水,充分溶解后,为饱和溶液的是________溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。下列说法正确的是________(填字母序号)。
A.溶质的质量不变
B.溶液中溶质的质量分数一定减小
C.溶液质量可能不变
D.可升高温度或增加溶剂
【答案】
【解析】
(1)根据活性炭的作用回答;
(2)硝酸钾溶液中溶质是硝酸钾;
(3)根据稀释前后溶质的质量不变进行解答;
(4)根据饱和溶液的概念及饱和溶液、不饱和溶液的相互转化解答.
解:(1)活性炭可吸附异味和色素、有毒气体,故答案为吸附;
(2)被溶解的是溶质,硝酸钾溶液中溶质是硝酸钾,故答案为硝酸钾或KNO3;
(3)溶液稀释前后溶质的质量不变.
设加入水的质量是X.
(300g×25%)=(300g+x)×15%
x=200g
故答案为200g;
(4)①60℃时,氯化钠的溶解度是37.3g,氯化铵的溶解度是55.2g,即100g水中最多溶解37.3g氯化钠,100g水中最多溶解55.2g氯化铵,所以形成的溶液氯化钠溶液是饱和溶液,氯化铵溶液是不饱和溶液,故答案为NaCl;
②A、既然剩余固体溶解,所以溶质的质量增加,故错误;
B、升高温度不能形成氯化钠的不饱和溶液,加入水,溶质的质量 不变,溶液的质量增加,质量分数一定减小,故正确;
C、溶质质量增加,溶液质量一定增加,故错误;
D、要使溶液中的溶质继续溶解,可采取增加溶剂的方法,升高温度不能让食盐水变不饱和,故错误.
故选B.


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:初中化学 来源: 题型:
【题目】下图表示部分元素的离子结构示意图和元素周期表的一部分。请回答:
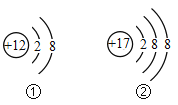
1 H 氢 1.008 | ||||||
8 O 氧 16.00 | 9 F 氟 19.00 | |||||
13 Al 铝 26.98 | 17 Cl 氯 35.45 | |||||
(1)写出图①所表示的离子符号___________;图①和图②所表示的离子形成化合物的化学式___________。
(2)从表中查出铝元素的相对原子质量为___________。
(3)在元素周期表中氟元素与氯元素位于同一纵行的原因是_________。
(4)表中原子序数为1、8的两种元素的常见单质反应的化学方程式为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~E分别是初中化学中常见的物质,它们之间的转化关系如下图所示,“一”表示物质之间能发生反应,A、B、D都是黑色固体,C、E是空气中的成分,A、E是单质,A和B反应有红色固体生成,A和D反应有铁生成。请回答下列问题:
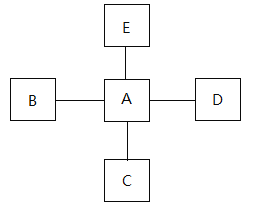
(1)写出物质B的化学式:__________;
(2)写出物质E的一种用途:_________;
(3)A和C反应的基本反应类型是__________;
(4)写出A和D之间发生反应的化学方程式:_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如下装置进行碳及其氧化物的性质研究,请回答相关问题:
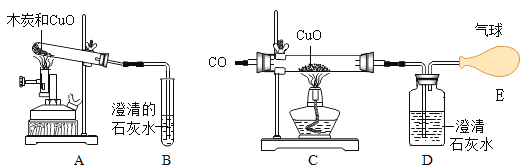
(1)图1:装置 A 中试管内木炭与氧化铜反应的现象是_____,反应的化学方程式是_____,具有还原性的物质是_____。实验结束时,立即趁热试管内固体倒在石棉网上,一段时间后,观察到 固体中又出现了黑色固体,原因是_____。
(2)图2:实验前先通一氧化碳,过点再点燃 C 处酒精灯,目的是_____,装置 C 中玻璃管内反应的化学方程式是_____。实验结束时先撤离 C 处酒精灯,待_____时停止通一氧化碳, 目的是_____。E 处加气球目的_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图所示实验分析得出的结论中,不正确的是( )
|
|
|
|
A.甲烷燃烧生成二氧化碳和水 | B.铁能在氧气中燃烧 | C.白磷的着火点比红磷的低 | D.二氧化碳的密度比空气大,不燃烧也不支持燃烧 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)阅读下面科普短文(原文作者:段翰英等)。
我国制作泡菜的历史悠久。制作泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成。泡菜品种繁多、风味独特、口感鲜脆。
蔬菜中含有硝酸盐。硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐[如亚硝酸钠(![]() )]与胃酸(主要成分是盐酸)反应,产生亚硝酸(
)]与胃酸(主要成分是盐酸)反应,产生亚硝酸(![]() )和氯化物(如
)和氯化物(如![]() )。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
泡菜中含亚硝酸盐吗?含量有多少?含量受什么因素影响呢?
经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。
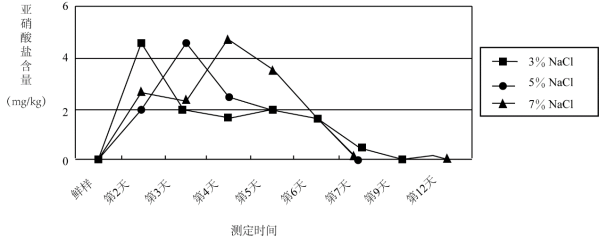
用不同的蔬菜进行测定,变化趋势与芹菜相似。
实验表明,发酵温度对泡菜中亚硝酸盐的生成量及生成时间也具有明显的影响。泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。这与温度较高有利于乳酸菌的繁殖有关。
实验还表明,泡制过程中添加姜汁和维生素C,都能有效地减少亚硝酸盐的生成。
现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。另外,泡制过程也会造成某些营养素的流失。(有删改)
依据文章内容,回答下列问题。
(1)泡菜中的亚硝酸盐是由 转化成生的。
(2)亚硝酸钠能与盐酸反应,该反应属于基本反应类型中的 反应。
(3)室温下,用芹菜制作的泡菜,最佳食用时间是 (填字母序号,下同)。
A.泡制2-3天 B.泡制5-6天 C.泡制12天后
(4)下列关于制作泡菜的说法中,合理的是 。
A.最好加入一些姜汁
B.最好在较低温度下泡制
C.最好加入一些富含维生素C的水果
D.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关
(5)请你为喜欢吃泡菜的人提一条食用泡菜的建议: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】把4g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示:
第一次 | 第二次 | 第三次 | |
氧气的质量(g) | 3 | 4 | 6 |
SO2的质量(g) | 6 |
请回答下列问题:
(1)写出此反应的化学方程式:_____;
(2)第一次实验中参加反应的硫、氧气和生成二氧化硫的质量之比是_____;
(3)通过计算,第二次实验生成二氧化硫的质量为_____;
(4)第三次生成的二氧化硫的质量为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学在老师的指导下,正确完成如下图所示两个实验。已知所用实验装置气密性良好。

关于该实验,有如下说法:①红磷熄灭并冷却后才能打开弹簧夹;②点燃酒精灯加入铜丝,可观察到铜丝有红色变成黑色;③停止加热后即可读出注射器内气体的体积约为24mL;④实验取用铜丝质量的多少不会影响实验结果;⑤两个实验均能证明空气是混合物;⑥两个实验均能证明空气中约含1/5体积的氧气。其中正确说法的个数有( )
A.2个 B.3个 C.4个 D.5个
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃,氯化钠的溶解度为36克/100克水。能证明下图烧杯中是氯化钠饱和溶液的实验是
A.称量溶液质量为136克
B.加入氯化钠,有固体不溶
C.恒温蒸发,有固体析出
D.测得溶质和溶剂的质量比为9:25
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com