
����Ŀ��ʵ������һƿ̼��ƺ��Ȼ��Ʒ�ĩ��ɵľ��Ȼ���С������ͬ��������������ϡ����û���ﷴӦ��������Һ��Ϊ��������Һ��������ʵ�����ݼ�¼�������������㣨д��������̣�
ʵ����� | һ | �� | �� | �� |
ϡ��������/g | 100.0 | 100.0 | 100.0 | 100.0 |
���������/g | 3.0 | 6.0 | 9.0 | 12.0 |
������Һ����/g | 101.9 | 103.8 | 105.0 | a |
ʣ���������/g | 0 | 0 | m | n |
��1����������̼��ƺ��Ȼ�������֮��__________
��2������a��ֵΪ_______��
��3�������m��ֵ__________��
���𰸡�5��1 105.5 1.25g
��������
����ͼ�������ݷ�����ÿ����3.0g������Һ����1.9g�������μ�������9.0g����Һ��������Ϊ5.0gС��1.9g��3��˵�������ʣ�࣬ϡ������ȫ��Ӧ�����һ������ϡ���ỹ��ʣ�ࡣ
��1���⣺�ɷ�������һ�����ݿ�֪�����ɶ�����̼������Ϊ100.0+3.0g��101.9g��1.1g
��3.0g�������̼��Ƶ�����Ϊx��
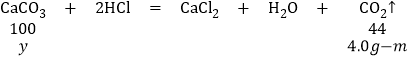
100��44=x��1.1g
x��2.5g
�������̼��ƺ��Ȼ�������֮��Ϊ2.5g����3.0g��2.5g����5��1
�𣺻������̼��ƺ��Ȼ�������֮��Ϊ5��1��
��2�����ڵ���������ʣ�࣬ϡ������ȫ��Ӧ�����Ե�����ȵ������ӵĻ���������Ϊ12.0g��9.0g��3.0g��3.0g������е��Ȼ�������Ϊ3.0g��2.5g��0.5g������a��105.0+0.5��105.5������105.5��
��3���⣺�������в���������̼������Ϊ100.0g+9.0g��105.0g��m��4.0g��m��
�跴Ӧ��̼��Ƶ�����Ϊy��
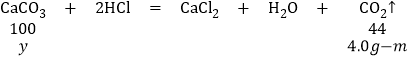
100��44=y��(4.0gm)�����y��![]() ��9.0g������е�̼�������Ϊ9.0g��
��9.0g������е�̼�������Ϊ9.0g��![]() ��7.5g������
��7.5g������![]() +m��7.5g��m��1.25g������1.25g��
+m��7.5g��m��1.25g������1.25g��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CuSO4Ϊԭ���Ʊ���ʽ̼��ͭ[Cu2(OH)2CO3]�Ĺ�����ͼ��
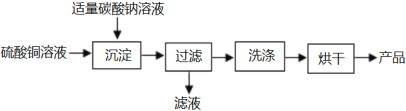
��1����������ʱ�ķ�ӦΪ2CuSO4+2Na2CO3+H2O=Cu2(OH)2CO3��+2______+CO2������������Ƿ�ϴ�Ӹɾ���Ӧѡ��______���BaCl2��Һ����ϡ���ᡱ����
��2�����ʱ��Ʒ�г���������ɫ���ʣ����ܵ�ԭ����______�������ᵼ�²�Ʒ�м�ʽ̼��ͭ����������___��������ƫ����������������ƫС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪA~G�����г������ʣ���ת����ϵ������A����Ȼ������Ҫ�ɷ֡�
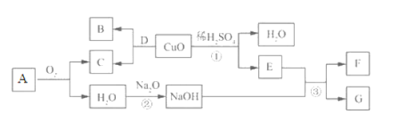
����������Ϣ�ش��������⣺
��1��д��A �Ļ�ѧʽ��________���䳣����;Ϊ_________________����дһ������
��2����Ӧ�ٵ�����Ϊ________________________________��
��3��д����Ӧ�ڵĻ�ѧ����ʽ _________________________���÷�Ӧ����_________��Ӧ���������Ӧ���ͣ���
��1��д����Ӧ�۵Ļ�ѧ����ʽ ___________________________________��
��2��Na2O��CaO�Ļ�ѧ�������ƣ�����������______________�����ţ�����Na2O������ѧ��Ӧ��
a.Mg b.N2 c.ϡ���� d.NaCl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾʵ�������ȷ���ǣ� ��
A. 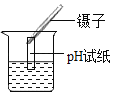 ����Һ��pHB.
����Һ��pHB. 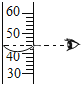 ����Һ�����
����Һ�����
C. 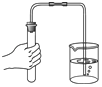 ���װ��������D.
���װ��������D. 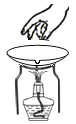 ����������
����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������ڷɣ����ڳ������������������⣬��ش�
��1���Ͻ��������ڵ�һ������������㷺Ӧ�ã���������Ҫ������Ǧ��������ɽ�����Ⱦ���_______�����ԣ������ں��ӵ���Ԫ����
��2���糵���������������ʱʹ�õĴ�����������_______���ϡ�
��3������������������������潫�γ���������Ĥ����Ч���ⸯʴ��Ϊ���顰������������������������Ƿ��γ���������Ĥ�������������������ͭ��Һ�У��������������ֺ�ɫ���ʣ��ɴ˿�֪�����������������Ч��_______����á����á�������Ϊ_______���û�ѧ����ʽ��ʾ����
��4������������Ҫ���Ĵ������������Ƚ���
����ҵ�ϳ��õ���������ķ���ұ�����������÷�Ӧ����_______������ĸ��ţ�
A ���Ϸ�Ӧ B �ֽⷴӦ C �û���Ӧ D ���ֽⷴӦ
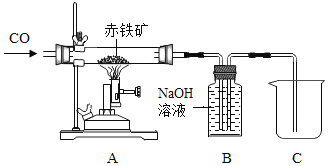
��ij��ȤС����ʵ����������CO����ģ��������ԭ������ͼ��ʾ��
��Ϊ�˱���װ��A�в������ڼ���ʱ���ܷ�����ը������ǰӦ_______��
��װ��A�������з�����Ӧ�Ļ�ѧ��Ӧ����ʽ��_______��
��װ��B��������_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ѳ�Ϊһ������ѧ�ƣ����������벻����ѧ��
��1��ʳ�������ĺ���Ʒ������Ϊ���岹����Ԫ��____��дԪ�ط��ţ���
��2������أ�KNO3���dz��õĸ��Ϸʣ����е�Ԫ�صĻ��ϼ�Ϊ____��
��3���ۻ���Ҫ�ɷ���As4S4��As�����Ԫ�ط��ţ�����As4S4�Ļ�ѧ������____��
��4�����ˮʵ��֤����ˮ����ɣ��÷�Ӧ�Ļ�ѧ����ʽ��____��ʵ���������˲���13mL���壬���˲�����������____mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ص���ˮ��Ϊ�����ṩ������ı�ݣ���ͼ��һ��ص���ˮ����ʾ��ͼ��
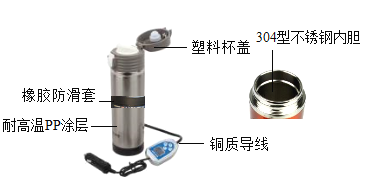
��1��ͼ�б�ʾ�������У����ںϽ����_____��ͭ���������������������_____���ʡ�
��2��ˮ���������µ�PPͿ�㲻�����ۣ����ҿ�����Ч��ֹ����_____����д���ʵĻ�ѧʽ���Ӵ������⡣
��3��Ϊ�˱Ƚ�����ͭ�Ľ�����ԣ�ijͬѧ��������·�����������ͭ�ֱ����2֧װ����������Һ���Թ��У��ȽϷ�Ӧ����Һ��ɫ�ı仯������Ϊ�÷���_____���������������������������_____��
��4�����ϡ����������������������е�����Խ��Խ���ɴ���Ի�ѧ��ʲô�µ���ʶ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ˮʵ��ʱ������ˮ�м���������������ǿ��Һ�ĵ����ԣ����������Ʊ��������ڵ��ˮ�Ĺ����з�����ѧ�仯���������Ƶ�����Ҳ���ᷢ���ı䡣�ֽ�8g�������Ƶ���Һ��101gˮ�в�ͨ�磬һ��ʱ�������1g��������ش��������⣺
(1)������0.7g����ʱ����������������ͬ�����µ������ԼΪ_______��
(2)�������У�����1g����ʱ�����ĵ�ˮ������Ϊ_______g��
(3)���ˮ�����У�������1g����ʱˮ��Һ���������Ƶ���������Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧѧϰ�У����dz�����ʶ�����ʵ��۽ṹ��
��1���Ȼ��ơ����ʯ���ɱ����������У������ӹ��ɵ�������_____
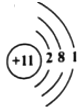
��2����ͼ��ij���ӵĽṹʾ��ͼ���������ڻ�ѧ��Ӧ����_____���ӣ���õ�����ʧȥ��������Ԫ�صĻ�ѧ���ʹ�ϵ�����е���ԭ�ӵ�_____.
��3����ͼ��A��B��C��D���������ӵĽṹʾ��ͼ��
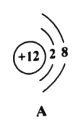
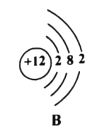
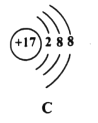

�ش��������⣺
��ͼ��A��B��C��D����_____��Ԫ�ص�����;
��A��B��C��D���������У����߱��ȶ��ṹ����_____������ţ���
��D��x=_____;
��A��C�γɻ�����Ļ�ѧʽ��_____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com