


科目:初中化学 来源:化学教研室 题型:038
磁铁矿的主要成分是四氧化三铁,赤铁矿的主要成分是三氧化二铁,它们都可以用来炼铁.
(1)
根据化学式计算,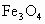 与
与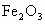 ,中铁元素的质量分数哪个大?
,中铁元素的质量分数哪个大?
(2)
现有160t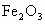 ,可炼出铁多少吨?
,可炼出铁多少吨?
(3)
若改用四氧化三铁来炼,需四氧化三铁多少吨才能得到相同质量的铁?查看答案和解析>>
科目:初中化学 来源: 题型:多选题
查看答案和解析>>
科目:初中化学 来源:沪教版九年级上《3.3 物质的组成》课时训练(2)(解析版) 题型:选择题
查看答案和解析>>
科目:初中化学 来源:《3.3 物质的组成》2013年同步练习(一)(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com