

分析 (1)含有Na+、Al3+、Fe3+等杂质的碳酸钙与盐酸反应后得到含有Ca2+、Na+、Al3+、Fe3+、Cl-、H+等离子的溶液,调节溶液的pH为8.0~8.5,使Al3+、Fe3+沉淀而除去,由流程图知加入氢氧化钙或通入氨气均不引入杂质.
(2)沉淀需要过滤分离,所以操作I为过滤,得到碳酸钙后需要加入盐酸使其转化为氯化钙溶液,氯化钙溶液经过蒸发浓缩、冷却、结晶则可得到CaCl2•2H2O晶体.过滤需要的玻璃仪器有玻璃棒、烧杯和漏斗.
(3)酸化操作是加入过量盐酸,调节溶液的pH为4.0,目的之一是为了将少量的Ca(OH)2转化为CaCl2.
(4)加入碳酸铵后,溶液中的钙离子与碳酸根离子结合生成碳酸钙沉淀;溶液2中含有铵根,铵盐可作化肥.
(5)考虑AgNO3溶液与氯离子反应生成氯化银沉淀.
(6)根据“称得沉淀质量为2.87g”,利用化学方程式进行计算上述样品中CaCl2•2H2O的质量分数;考虑样品中有少量氯化钠.
解答 解:(1)含有Na+、Al3+、Fe3+等杂质的碳酸钙与盐酸反应后得到含有Ca2+、Na+、Al3+、Fe3+、Cl-、H+等离子的溶液,调节溶液的pH为8.0~8.5,使Al3+、Fe3+沉淀而除去,由流程图知加入氢氧化钙或通入氨气均不引入杂质,故答案为b.
(2)沉淀需要过滤分离,所以操作I为过滤,得到碳酸钙后需要加入盐酸使其转化为氯化钙溶液,氯化钙溶液经过蒸发浓缩、冷却、结晶则可得到CaCl2•2H2O晶体.过滤需要的玻璃仪器有玻璃棒、烧杯和漏斗.
(3)酸化操作是加入过量盐酸,调节溶液的pH为4.0,目的之一是为了将少量的Ca(OH)2转化为CaCl2.
(4)加入碳酸铵后,溶液中的钙离子与碳酸根离子结合生成碳酸钙沉淀,故加入碳酸铵所发生的反应的方程式:CaCl2+(NH4)2CO3=CaCO3↓+2NH4Cl,溶液2的一种用途作氮肥.
(5)测定样制得品中Cl-含量的方法是:称1.5g样品,溶解,滴加过量的 AgNO3 溶液,过滤、洗涤、干燥,称得沉淀质量为2.87g,证明沉淀洗净的标准是:取最后一次洗涤的滤液,滴加 NaCl试剂,若 无明显现象,则已经洗净.
(6)根据“称得沉淀质量为2.87g”,设样品中CaCl2•2H2O的质量为x,
CaCl2•2H2O+2AgNO3=Ca(NO3)2+2AgCl↓+2H2O
147 287
x 2.87g
则$\frac{147}{287}=\frac{x}{2.87g}$,解得x=1.47g,故样品中CaCl2•2H2O的质量分数为:$\frac{1.47g}{1.5g}×100%$=98%.
若用上述方法测定的样品中CaCl2•2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有:样品中有少量氯化钠.
故答案为:
(1)b; (2)过滤; 降温结晶;烧杯;(3)Ca(OH)2; (4)CaCl2; 作氮肥;
(5)NaCl(或者Na2CO3,合理即可);无明显;(6)98%;样品中有少量氯化钠(或少量晶体失水)
点评 本考点属于物质的分离和提纯,考查氯化钙晶体制备工艺流程的有关判断,是中考的重点也是一个难点,物质的溶解性要记牢,还要加强记忆除去常用离子和特殊离子的方法,从而突破难点.根据物质的溶解性和除杂质的条件,要认真分析,综合把握.


科目:初中化学 来源: 题型:选择题
| A. | 煤燃烧时向煤炉中鼓入空气 | B. | 面团发酵时放在温热处 | ||
| C. | 某些食品密封包装时充入氮气 | D. | 用双氧水制氧气加入二氧化锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫和氧 | B. | 氢和氧 | C. | 只有硫 | D. | 氢、硫、氧 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气、冰水混合物、空气 | B. | 氮气、过氧化氢溶液、钢 | ||
| C. | 冰、干冰、生石灰 | D. | 金刚石、熟石灰、石油 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 反应前后原子种类、数目均不变 | B. | 该反应中各物质均为化合物 | ||
| C. | 该反应中,反应物的质量比是1:2 | D. | 该反应为置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
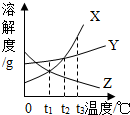 如图表示X、Y、Z三种物质的溶解度曲线,下列说法正确的是C
如图表示X、Y、Z三种物质的溶解度曲线,下列说法正确的是C查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 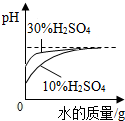 稀释等质量溶质质量分数分别为30%和10%的H2SO4溶液 | |
| B. | 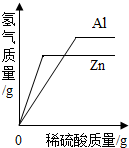 等质量的Al、Zn与足量的等溶质质量分数的稀硫酸反应 | |
| C. | 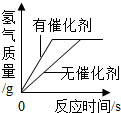 用等质量、等容质质量分数的过氧化氢溶液分别制取氧气 | |
| D. | 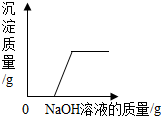 向氯化铜和硝酸铜的混合溶液中滴加氢氧化钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com