
| A. | 铁粉 | B. | FeCl3溶液 | C. | NaCl溶液 | D. | Na2CO3溶液 |
分析 根据NaOH、AgNO3和KNO3的性质,分析三种物质溶液分别与所提供的四种试剂反应的情况,判断能一次性鉴别出三种溶液的试剂要求必须出现不同的现象.
解答 解:A.铁粉只能和AgNO3混合反应,和NaOH和KNO3混合都无现象,因此无法鉴别出KNO3、NaOH溶液,故选项错误;
B.FeCl3溶液加入三种溶液中依次出现的现象是:生成红褐色沉淀、白色沉淀、无明显现象,可鉴别,故选项正确;
C.氯化钠只能和硝酸银反应产生沉淀,不能鉴别KNO3、NaOH溶液,故选项错误;
D、Na2CO3溶液不与KNO3、NaOH溶液反应,无现象,因此不能鉴别NaOH和KNO3,故选项错误;
故选B.
点评 本题考查了常见物质的鉴别题,在解此类题时,首先分析需要鉴别的物质的性质,然后选择适当的试剂,出现不同的现象即可鉴别.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案科目:初中化学 来源: 题型:解答题
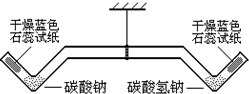 西园中学化学兴趣小组在老师指导下,对碳酸钠、碳酸氢钠的性质作进一步探究.
西园中学化学兴趣小组在老师指导下,对碳酸钠、碳酸氢钠的性质作进一步探究.| 实验现象 | 实验结论 | |
| ①用酒精灯加热左端的碳酸钠2min | 长柄双V管保持水平,干燥的蓝色石蕊试纸不变色 | 碳酸钠受热不分解 |
| ②再加热右端的碳酸氢钠2min | 长柄双V管右端上升,干燥的蓝色石蕊试纸变成红色 | 碳酸氢钠受热分解成碳酸钠等物质,有关的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 化学能帮助我们更好地认识生活、改善生活.
化学能帮助我们更好地认识生活、改善生活.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
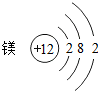 镁是一种用途广泛的金属,其原子结构如图所示,下列说法错误的是( )
镁是一种用途广泛的金属,其原子结构如图所示,下列说法错误的是( )| A. | 质子数为12 | B. | 最外层电子数为2 | ||
| C. | 易失去电子形成阴离子 | D. | 有三个电子层 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 海水中蕴含含有80多种元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氧气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.
海水中蕴含含有80多种元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氧气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
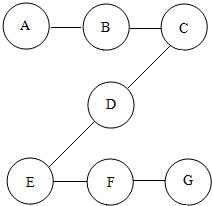 智能手机屏幕解锁图形如图所示.若A、B、C、D、E、F、G分别是铁丝、碳粉、二氧化碳、氧化铁粉末、稀硫酸溶液、氢氧化钙溶液、硝酸铜溶液中的一种,其中A为黑色物质,G为红色物质.(“-”相连两物质能发生反应)请完成下列各题:
智能手机屏幕解锁图形如图所示.若A、B、C、D、E、F、G分别是铁丝、碳粉、二氧化碳、氧化铁粉末、稀硫酸溶液、氢氧化钙溶液、硝酸铜溶液中的一种,其中A为黑色物质,G为红色物质.(“-”相连两物质能发生反应)请完成下列各题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com