
【题目】下面是几种实验室制取气体的发生装置和收集装置,请回答下列问题:
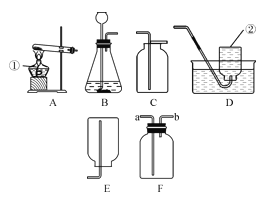
(1)写出仪器的名称:①_______,②_______;
(2)实验室用过氧化氢制取氧气时应选用的发生装置是_____(填字母,下同),收集装置是_____,该反应的化学方程式是_________;
(3)用B装置制取二氧化碳时,长颈漏斗伸入液面下的原因是____________;
(4)F是一种可用于集气、洗气等多功能装置,若将F装置内装满水来收集氧气,则气体应从______(填“a”或“b”)进入F中。
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:初中化学 来源: 题型:
【题目】在现代生活中,人们越来越注重微量元素的摄取.碘元素对人体有着至关重要的作用。下图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答下列问题:

(1)食用“碘盐”属于______(纯净物或混合物);
(2)碘酸钾(KIO3)中碘元素的化合价为______;
(3)上述“含碘量”中的碘是指______。
①碘酸钾②碘元素③碘单质④碘分子
(4)由上述“文字说明”可推测碘酸钾的一种化学性质是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种物质的溶解度曲线,据图回答:
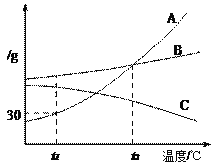
(1)t1℃时A、B、C三种物质的溶解度由大到小的顺序是___________(填写序号,下同)。
(2)t1℃时30gA物质加入到50g水中不断搅拌,形成的溶液质量是_________g。
(3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大小关系是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤属于不可再生能源,将煤通过一定方式可转化为汽油,乙醇(C2H5OH)和气体燃料。乙醇可用作燃料,我国已经推广使用一种车用乙醇汽油,这种汽油的燃烧废气对环境的污染较少。请计算:
(1)69g乙醇完全燃烧,生成二氧化碳的质量为多少?(要求写出计算过程)
(2)在氧气不足的情况下,乙醇不完全燃烧生成一氧化碳、二氧化碳和水,若69g乙醇不完全燃烧生成88g二氧化碳,则反应生成一氧化碳和水的分子个数比为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据你的所学,请回答有关问题:
(1)用一个空的软塑料瓶收集一瓶二氧化碳气体,在瓶中倒入1/3容积的水,立即盖紧瓶振荡,观察到塑料瓶变瘪了,该现象说明二氧化碳具有的性质是__________________
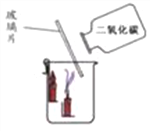
(2)如图,从烧杯的一侧倾倒二氧化碳,观察到的现象是_________________,该实验说明二氧化碳_______________的物理性质和_________________的化学性质
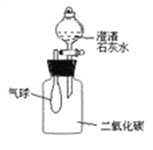
(3)如图,准备好双孔塞(插有带小气球的短玻璃管和盛有澄清石灰水的分液漏斗)取装满二氧化碳的集气瓶,用双孔塞将集气瓶塞紧。把澄清石灰水放入集气瓶振荡,可观察到的现象是________、_______其原因是____________(用化学方程式表示)
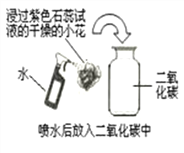
(4)某同学用石蕊试液染成紫色的干燥的小花做了两个实验:
实验一:把干燥的小花直接放到干燥二氧化碳的集气瓶中,无现象产生,说明__________________
实验二:用水喷湿后放入装有二氧化碳的集气瓶里(如图示),可观察到的现象__________其原因是________________(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图回答问题。

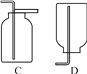
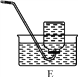
(1)实验仪器a的名称是_____;仪器b的名称是_____。
(2)实验室用高锰酸钾制取氧气的化学方程式为____________,可选用的发生装置是___(填字母序号,下同)。用E装置收集氧气的原因是_________。
(3)氢气是一种无色、无味,难溶于水的气体,其密度比空气的密度小,在实验室中常用金属锌粒和稀硫酸(H2SO4)反应制取,生成硫酸锌(ZnSO4)和氢气。
①实验室制取氢气的发生装置是___,收集装置是_____;制取氢气的化学方程式为_______;
②氢气与氧气混合点燃可能会发生爆炸,因此点燃之前必先_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是元素周期表的一部分,请回答下列问题。
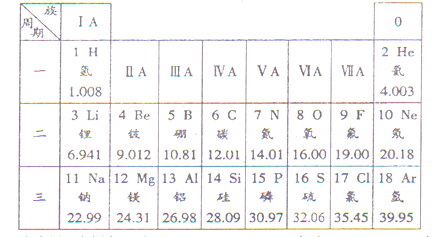
(1)以氟元素为例,方框中“9”表示____________,“19.00”表示___________________,一个氟原子中有 _________个中子,氟原子在化学反应中易 ________(填“得到”或“失去”)电子。
(2)周期表中,如3~10号元素组成的横行叫________,如1、3、11号元素组成的纵行称_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用100 g KClO3和MnO2的混合物,测得MnO2 占混合物总质量的25%。
求:(1)混合物中氧元素的质量分数是多少(计算过程中保留两位小数)。
(2)如果给混合物加热使其发生反应,一段时间后,测得剩余物质含有KClO3、MnO2和KCl,其剩余物质的总质量为95克。求此剩余物质中Mn元素的质量分数?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
在中国古代化工发展的历史征程中,我国古代先民们在火药、制陶烧瓷、炼铜冶铁等化学加工技术方面取得了许多非凡的成就,为促进我国古代社会发展和人类的进步做出了重大的贡献。
【火药】人类最早使用的火药是黑火药,主要反应如下:

【制陶烧瓷】瓷器与陶器,都属于硅酸盐系列制品,最主要的化学成分是二氧化硅(SiO2)、氧化铝(Al2O3)及多种金属(Ca、Mg、Fe、K、Na等)氧化物。但在化学成分含量、用途等方面却大有区别。
制品 | 化学成分 | 性能用途等 |
陶器 | Al2O3 约15%~18%; Fe2O3约5%~6%; CaO、MgO等≥3%。 | 粗糙,不够坚硬,常用于取水、盛放食物等。 |
瓷器 | Al2O3 约18%~28%; Fe2O3约1%~2%; CaO、MgO等≤1%。 | 高温烧结,坚硬致密,洁白,薄, 呈半透明,敲击时清脆悦耳,美观,用途广泛,观赏、收藏价值高等。 |
【金属冶炼】制陶发展起来的高温技术为金属的冶炼、熔铸创造了条件,我国由新石器时代晚期逐步进入了先是炼铜(称为“青铜器时代”)后是炼铁(称为“铁器时代”)的金属时代。
青铜冶炼
天然铜夹杂在铜矿石之中,人们在加热熔化天然铜的过程中,将绿色的孔雀石[Cu2(OH)2CO3]、棕或黑色的锡石(SnO2)、蓝色的方铅矿(PbS)放在一起烧,便产生了青铜。青铜是铜与锡或铅熔成的合金。熔点比纯铜(1083℃)低100℃~300℃,更易加工和铸造,铸造性能也比纯铜好,硬度几乎提高一倍,适合制作工具和兵器。
铁的冶炼
到了春秋中后期,我国先民们在熟悉地掌握了块炼法炼铁后,又在世界上率先发明了以高温液体还原法冶炼生铁的技术,这在冶金史上是一个划时代的进步。
随着炼铁技术的进步,人们也逐渐懂得了炼钢。生铁和钢都是铁碳合金。含碳量>2%,为生铁;含碳量<0.02%,为纯铁;含碳量在两者之间为钢。依据文章内容回答下列问题。
(1)黑火药的主要成分是________。
(2)陶器与瓷器化学成分的主要区别是_________。
(3)生铁的碳含量______(填“高于”或“低于”)钢的碳含量。
(4)与纯金属相比,合金的优点可能是________。
【答案】 硝酸钾、木炭、硫(KNO3 、C、S) 陶瓷中Al2O3含量比瓷器低,Fe2O3、CaO、MgO含量比瓷器高 高于 硬度大、熔点低
【解析】本题考查了根据短文黑火药、陶器与瓷器化学成分,铁合金的成分和性质,认真阅读短文是解题的关键。
(1)从题中提供的化学方程式可知,黑火药的主要成分是硝酸钾、木炭、硫(KNO3 、C、S);
(2)根据陶器与瓷器化学成分表可知,陶器与瓷器化学成分的主要区别是:陶瓷中Al2O3含量比瓷器低,Fe2O3、CaO、MgO含量比瓷器高;
(3)生铁和钢都是铁碳合金。含碳量>2%,为生铁;含碳量<0.02%,为纯铁;含碳量在两者之间为钢。生铁的碳含量高于钢的碳含量;
(4)与纯金属相比,合金的优点可能是:硬度大、熔点低。
【题型】简答题
【结束】
21
【题目】工业上制取硝酸铵(NH4NO3)的流程图如下,请回答下列问题。
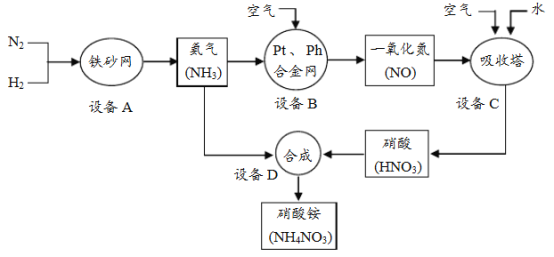
(1)设备A中,发生的反应属于基本反应类型中的________。
(2)设备B、C中,空气中的______一定参加了反应。
(3)设备C中,生产硝酸过程排出的废气中会含有一些氮的氧化物,可用如下两种
方法处理:
方法一、NaOH溶液吸收法:NO + NO2 + 2NaOH = 2NaNO2 + H2O
方法二、NH3还原法:8NH3 + 6NO2![]() 7N2 + 12H2O(NO也有类似的反应)
7N2 + 12H2O(NO也有类似的反应)
以上两种方法中,你认为哪种方法好并说明理由________。
(4)设备D中,用NH3和HNO3制备NH4NO3。NH4NO3中氮元素质量分数的计算式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com