
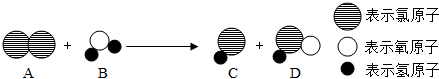
分析 (1)根据提供的信息可判断A是Cl2分子,B是H2O分子,生成物C是HCl分子,D是HClO,可检验有盐酸生成可用硝酸银溶液,然后根据反应物和生成物书写化学方程式.
(2)根据预防传染病的措施分析回答.
解答 解:(1)通过提供的原子模型和反应的示意图,可分析出反应物的氯气和水,生成物是氯化氢和次氯酸,检验盐酸的方法是在反应后的溶液里滴几滴AgNO3溶液,盐酸和硝酸银反应能生成白色的氯化银沉淀,化学方程式为 HCl+AgNO3=AgCl↓+HNO3;
(2)对周围环境采取严格的消毒,从预防传染病的措施看属于切断传播途径.
故答案为:(1)HCl+AgNO3=AgCl↓+HNO3;(2)切断传播途径.
点评 解答时要充分理解图中提供的信息和书写化学方程式的方法,并能够根据示意图判断分子的构成.


科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验某气体是否为CO2 | 将燃着的木条伸入气体中 |
| B | 鉴别NaCl溶液和稀盐酸 | 滴加无色酚酞溶液 |
| C | 除去CaCO3中的Na2CO3 | 加水溶解,过滤 |
| D | 除去CO2中的CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
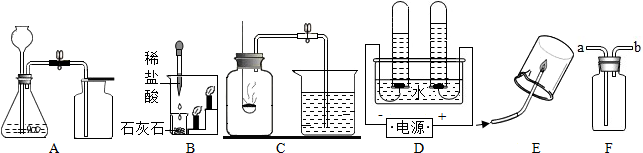
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
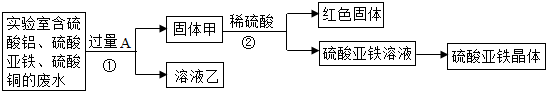
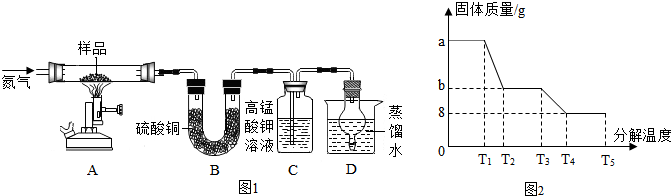
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 291 | B. | 174 | C. | 117 | D. | 57 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
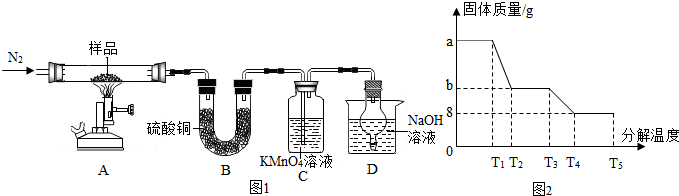
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 向某固体中加入稀盐酸有气泡产生,可证明该物质一定是CO32- | |
| B. | 分别将镁、铁、铜、银放入稀盐酸中,可确定它们的活动性顺序 | |
| C. | 常温下可用铁与氯化银反应制取银 | |
| D. | 可用过量的氢氧化铜除去硫酸铜溶液中少量的硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com