
【题目】中国古代在认识和应用物质方面有辉煌的历史,请用恰当的化学用语填空。
(1)《本草纲目》中“灶中所烧薪柴之灰,令人以灰淋汁,取碱涴衣”中的碱为草木灰_____;
(2)《本草钢目》中“水银乃至阴之毒物,因火煅丹砂而出”水银的化学式_____;
(3)《报朴子)中记载“曾青涂铁,铁赤如铜”其曾青指硫酸铜溶液,其阳离子为_____;
(4)《天工开物》中“凡石灰,经火焚炼为用”的石灰主要成分为碳酸钙_____。
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】2022年第24届冬季奥林匹克运动会将在我国北京-张家口举办。
(1)下列冬奥会事项与化学无关的是_____________
A 研制新型材料用于场馆建设 B 在短道速滑的冰道上洒水减少摩擦
C 用消毒剂处理奥运村生活污水 D 用清洁能源做汽车燃料接送运动员

(2)造雪机的工作原理如图所示。A处空气被压缩,体积变小。从微粒的角度解释其原因是__。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示的四个图象分别对应四种过程,其中正确的是( )

A. ![]() 将NaOH溶液逐滴滴加到盛有稀
将NaOH溶液逐滴滴加到盛有稀![]() 的烧杯中
的烧杯中
B. ![]() 分别向等质量且足量的Mg和Zn中加入等质量,等浓度的稀硫酸
分别向等质量且足量的Mg和Zn中加入等质量,等浓度的稀硫酸
C. ![]() 室温时,向一定量的饱和石灰水中加入少量氧化钙
室温时,向一定量的饱和石灰水中加入少量氧化钙
D. ![]() 向
向![]() 溶液中逐滴加入稀硫酸
溶液中逐滴加入稀硫酸
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面相关信息,根据要求回答问题:
铁是目前世界上应用最广泛的金属,年产量位居第一。无论是日常生活用品,还是工农业生产或其他领域,都离不开铁。实验室中常用的还原铁粉,灰色或黑色粉末,又称“双吸剂”,常用于食品保鲜。还原铁粉一般由四氧化三铁在高温条件下,通入一氧化碳气流还原生成,其主要成分为结构疏松的单质铁,由于还原铁粉本身已是粉末状,再加之其微观结构又十分疏松,所以其应用更加广泛;另外,还原铁粉在化工生产及实验室作业中常用作优质还原剂。
(1)常见的铁制品大多是生铁或钢、不锈钢制成的,生铁和钢都是铁的_____。
(2)铁常被用来压成薄片或拉成细丝,这主要利用了铁的_____性。
(3)还原铁粉常用于食品保鲜,主要是因为能够吸收空气中的_____。
(4)在实验室中,用等质量的细铁丝和还原铁粉分别与等体积、等溶质质量分数的稀盐酸反应,还原铁粉与稀盐酸的反应更剧烈,原因是_____。
(5)用四氧化三铁制取还原铁粉的化学方程式是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图仪器或装置回答问题:
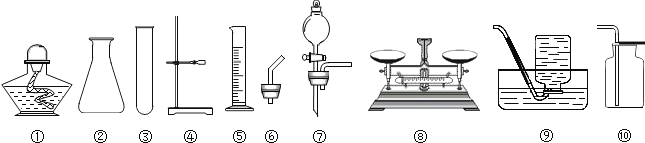
(1)写出仪器名称:②_____,⑤_____。
(2)用氯酸钾制取氧气,发生装置可选择图中的_____(填标号)进行组装,该反应的化学方程式是_____。
(3)实验室可将②⑦与_____(填标号)连接制取并收集二氧化碳,该发生装置与②⑥组装成的发生装置相比较,具有的优点是_____。
(4)某同学欲配制50g溶质质量分数为20%的氯化钠溶液,除了药匙、滴管、烧杯、玻璃棒外,还需用到上述仪器中的_____(填标号)。他在量取所需水的体积时,若仰视凹液面最低处读数,则所配置溶液中溶质的质量分数比20%_____(填“偏大”、“偏小”或“相等”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向硝酸铜和硝酸银混合溶液中加入一定量的铁粉充分反应后过滤,下列说法中正确的_____。
A.滤液中一定没有Ag+、Cu2+
B.滤液中一定有Fe2+
C.反应后溶液质量变大
D.滤渣中一定有_____(填化学式)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小杜为测定某粗盐(只含难溶性杂质)中氯化钠的含量,进行了实验。
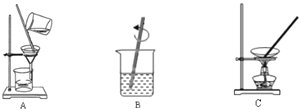
(1)操作的正确顺序是_______________________,其中过滤中玻璃棒的作用是_________。
(2)用托盘天平称量未知质量的粗盐固体时,发现天平指针偏左,应________(填序号)。
A增加适量砝码B减少适量砝码C增加适量粗盐固体
(3)如果A中的滤液仍然浑浊,应该__________________。蒸发操作中,当观察到蒸发皿中出现_______________时,停止加热。
(4)如果所测得的粗盐中氯化钠质量分数小于实际值,你认为可能的原因有(______)
A过滤时滤纸破损B未溶解充分就进行过滤
C蒸发过程中没有搅拌,有液滴飞溅D称量精盐质量时,左托盘放砝码
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在氢氧化钠溶液和稀盐酸的反应中,小明和老师用数字化设备测定了溶液温度及pH值随时间变化变化的关系曲线图。
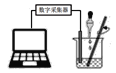

(1)根据曲线图,可知该实验是将_______(选填“氢氧化钠溶液”或“稀盐酸”)滴加到另外一种试剂中。该反应为___________。
A 吸热反应 B 放热反应
(2)a为温度曲线上的最高点,a、b两点对应的时间相同,则b对应的纵坐标数值为____。
(3)分别取样,依次进行以下实验:
①将b点处溶液中的溶质结晶,采用__________方法。
②取c点样品于试管中,加足量水稀释后溶液的pH__________7(填“>”、“<”或“=”)。
(4)若发现氢氧化钠溶液试剂瓶敞口放置,经检验该试剂中含有碳酸钠,请设计实验检验该样品中仍含有氢氧化钠_______。
(5)将50g稀盐酸加入50g氢氧化钠溶液中恰好完全反应,所得溶液中溶质的质量分数为5.85%。试计算氢氧化钠溶液中溶质的质量分数_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在学习盐酸的化学性质时,小红、芳芳两位同学分别作了碳酸钠溶液和稀盐酸反应的实验如图所示。
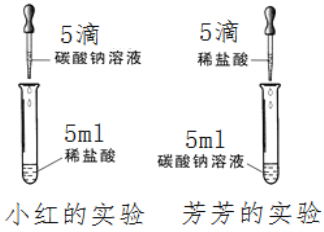
【实验现象】小红在实验中观察到有气泡冒出,而芳芳
所做的实验无现象。写出小红实验的化学反应方程式:________________。
【实验讨论】芳芳同学的试验为什么观察不到有气泡?
反应后溶液的溶质有哪些?
【查阅资料】①碳酸钠和稀盐酸反应生成物受到盐酸的质
量影响,稀盐酸过量生成二氧化碳,若盐酸量不足则生成碳酸氢钠;②碳酸氢钠与氯化钙溶液混合不发生反应,而碳酸钠和氯化钙溶液反应生成沉淀,且碳酸钠和碳酸氢钠溶液都呈碱性,氯化钙溶液呈中性。
【猜想与假设】实验反应后溶液中溶质可能有:①NaHCO3、NaCl、Na2CO3; ②NaHCO3、NaCl;
③NaHCO3、NaCl、HCl。
芳芳同学认为猜想③肯定不成立,理由是______________。
【实验设计】确定芳芳同学实验是否生成碳酸氢钠,并证明反应后的产物。
实验步骤 | 实验现象 | 实验结论 |
A、取上述溶液少量于试管中,加 入足量的________溶液。 | 产生白色沉淀 | 猜想①正确 |
B、取步骤A所得上层清液少量,滴加_______溶液。 | ___________ |
【实验反思】若用少量的稀盐酸鉴定氢氧化钠是否变质,发现无气泡冒出,则证明氢氧化钠溶液没有变质。对此实验结论,你是否赞同?若不赞同,还需说明理由。_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com