
【题目】化学源于生活,与工农业生产密切相关。
(1)用碳素墨水书写的文字很长时间不变色,是因为______;
(2)铁制品锈蚀是铁与空气中的_______、水蒸气等发生了化学变化,我们可以用稀盐酸去除铁制品表面的铁锈,其除锈的化学方程式为___________;
(3)下列化学肥料属于复合肥的是____(填序号);
①NH4H2PO4 ②(NH4)2SO4 ③KCl
(4)豆腐、鸡蛋、瘦肉等食物为人体提供的主要营养素是_____。
【答案】常温下,碳的化学性质很稳定 氧气 ![]() ① 蛋白质
① 蛋白质
【解析】
(1)在常温下,碳的化学性质很稳定,碳受日光照射或与空气、水分接触,都不容易起变化,故用碳素墨水书写的文字很长时间不变色,故填:常温下,碳的化学性质很稳定;
(2)铁生锈的条件是铁与氧气、水接触,故铁制品锈蚀是铁与空气中的氧气、水蒸气等发生了化学变化;
铁锈的主要成分是三氧化二铁,三氧化二铁能与稀盐酸反应生成氯化铁和水,该反应的化学方程式为:![]() ;
;
(3)①NH4H2PO4中含N、P两种营养元素,属于复合肥;
②(NH4)2SO4含氮元素,属于氮肥;
③KCl含钾元素,属于钾肥。
故属于复合肥的是①;
(4)豆腐、鸡蛋、瘦肉都富含蛋白质,故豆腐、鸡蛋、瘦肉等食物为人体提供的主要营养素是:蛋白质。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图是实验室制取并验证某种气体化学性质的有关装置,据此回答下列问题:
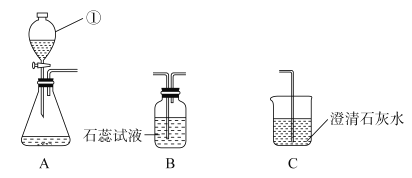
(1)仪器①的名称是_________;
(2)组装好装置A后,必须首先_________。
(3)若A与C连接,C中澄清的石灰水变浑浊,则实验室制取该气体的化学方程式是__________,用_________法收集该气体。
(4)若A与B连接,则B中紫色石蕊试液变_______色。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组用如图所示装置做酸碱中和反应实验。用胶头滴管吸取盐酸逐滴加入烧杯中,当溶液刚好由红色变成无色时,停止加入盐酸。
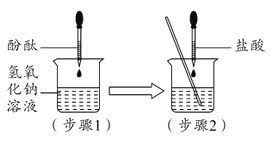
(1)写出有关反应的化学方程式_______。
(2)实验过程中,某同学不小心又多加了几滴盐酸,若要除去过量的盐酸,请写出可选用的试剂_______。
(3)中和反应在实际中具有广泛的应用,请举出一个实例_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线。

①t1℃时,甲的溶解度______乙的溶解度(选填“>”、“<”或“=”)。
②t2℃时,甲溶液从状态Q变成状态P,可采用的方法______(填写一种即可)。
③甲、乙、丙各50g分别加入到三只盛有100g水的烧杯中,充分搅拌,在t2℃时所得溶液的溶质质量大小关系是___。将此时所得的乙溶液降温,则溶液中溶质质量分数___(选填“变大”、“变小”或“不变”)。
④说法正确的是___。
A t1℃时,甲、丙一定能配得质量分数相等的两种溶液
B t1℃时,甲、乙饱和溶液分别升温到t2℃时,两者的溶质质量分数相等
C t2℃时,处于Q点状态的丙物质溶液中溶质质量为30g
D t2℃时,向处于P点状态的乙物质溶液中加水可变成Q状态
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质在水中的溶解度曲线。以下说法正确的是( )
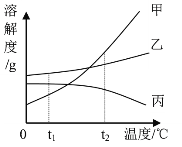
A.在t2℃时溶解度由大到小的顺序是乙>丙>甲
B.甲、乙、丙的饱和溶液分别由t2℃降到t1℃时,析出晶体最多的是甲溶液
C.甲、乙、丙的饱和溶液分别由t2℃降到t1℃时,丙溶液浓度一定不发生变化
D.甲、乙、丙三种物质的溶解度都随温度升高而增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明在实验室发现一瓶未知浓度的氢氧化钠溶液,为方便以后使用,他对其浓度进行了测定。取20g此氢氧化钠溶液于烧杯中,逐滴滴加溶质质量分数为9.8%的稀硫酸,并随时对反应后的溶液用pH计(一种测定溶液pH的仪器)测定溶液的pH,所得数据如下表:
加入稀硫酸的质量/g | 9.6 | 9.8 | 9.9 | 10 | 10.1 |
溶液的pH | 12.4 | 12.1 | 11.8 | 7 | 2.2 |
(1)当滴加稀硫酸的质量为9.8g时,溶液中的溶质有__________;
(2)计算所测氢氧化钠溶液中溶质的质量分数_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化铵和硝酸钾溶解度曲线如下图所示,下列叙述正确的是
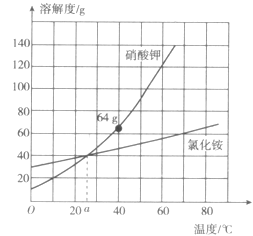
A.50℃时,氯化铵的溶解度大于硝酸钾
B.a℃时,氯化铵与硝酸钾溶液的质量分数相等
C.将60℃的硝酸钾饱和溶液降温变为不饱和溶液
D.40℃时,50 g水中加入50 g硝酸钾,充分搅拌,得到质量分数约为39%的硝酸钾溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用电石渣[主要成分为Ca(OH)2、MgO]制备硫酸钙的主要工艺流程如下:
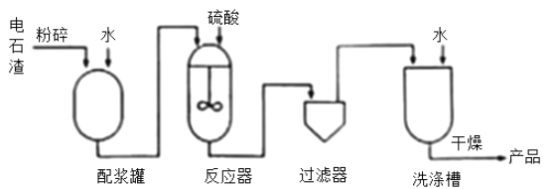
己知:MgO难溶于水;MgSO4易溶于水;CaSO4微溶于水。
(1)反应器中搅拌的目的是__________________________________________________。
(2)反应器中发生的反应主要有MgO+H2SO4=MgSO4+H2O和____________________。
(3)上述流程中,用于分离提纯的设备有______________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了测定某纯碱样品(含少量氯化钠杂质)中碳酸钠的质量分数,取该样品11g完全溶于100g水中,再向其中逐滴加入200g溶质质量分数为20. 8%的氯化钡溶液,生成沉淀的质量与加入氯化钡溶液的质量关系如下图。

请计算:
(1)图中m的值为__________。
(2)恰好完全反应时所得溶液溶质质量分数为多少_______?(请写出计算过程,结果精确到0.1%)
(3) 当氯化钡溶液滴加到50g时,则所得溶液中钠元素的质量为________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com