
·ÖĪö £Ø1£©øł¾ŻČ¼ĮĻŗ¬ÓŠĢ¼ŌŖĖŲ£¬²»ĶźČ«Č¼ÉÕŹ±»įÉś³ÉŅ»Ńõ»ÆĢ¼·ÖĪö£»
£Ø2£©øł¾Ż»ÆŹÆČ¼ĮĻµÄÖÖĄą·ÖĪö»Ų“š£»
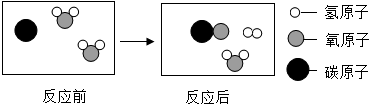
øł¾Ż·“Ó¦µÄĪ¢¹ŪŹ¾ŅāĶ¼¼°ÖŹĮæŹŲŗć¶ØĀÉ·ÖĪö·“Ӧɜ³ÉĪļµÄ·Ö×ÓøöŹż±Č£®
½ā“š ½ā£ŗ£Ø1£©Ćŗŗ¬ÓŠĢ¼ŌŖĖŲ£¬²»ĶźČ«Č¼ÉÕĪ²ĘųÖŠŗ¬ÓŠÉŁĮæŅ»Ńõ»ÆĢ¼£¬Ņ»Ńõ»ÆĢ¼ÓėŃŖŗģµ°°×½įŗĻČĆČĖÖŠ¶¾£»
£Ø2£©³£¼ūµÄ»ÆŹÆČ¼ĮĻ°üĄØĆŗ”¢ŹÆÓĶŗĶĢģČ»Ęų£®
ÓÉ·“Ó¦µÄĪ¢¹ŪŹ¾ŅāĶ¼¼°ÖŹĮæŹŲŗć¶ØĀÉæÉÖŖ£¬øĆĶ¼Ź¾ÖŠŅ»øöĢ¼Ō×ÓÓėŅ»øöĖ®·Ö×Ó·“Ó¦£¬Éś³ÉĮĖŅ»øöŅ»Ńõ»ÆĢ¼·Ö×ÓŗĶŅ»øöĒā·Ö×Ó£¬ĖłŅŌ£¬øĆ·“Ӧɜ³ÉĪļµÄ·Ö×ÓøöŹż±ČĪŖ1£ŗ1£®
¹Ź“š°øĪŖ£ŗ£Ø1£©Ņ»Ńõ»ÆĢ¼£Ø2£©ĢģČ»Ęų£»1£ŗ1£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĮĖ»ÆŹÆČ¼ĮĻµÄÖÖĄą£¬ĆŗµÄĄūÓĆ£¬ŹōÓŚ»ł“”µÄÖŖŹ¶£¬ÄŃ¶Č²»“ó£®øł¾ŻŅŃÓŠµÄÖŖŹ¶¼“æɽā“š£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® |  | B£® |  | C£® |  | D£® |  E£® E£® | ||||
| E£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÕĘųÄܱ»Ń¹Ėõ ·Ö×ÓĢå»żæÉŅŌ±äŠ” | |
| B£® | øŹÕįĢš£¬æą¹Ļæą ²»Ķ¬·Ö×ÓŠŌÖŹ²»Ķ¬ | |
| C£® | ½į±łµÄĖ®²»ÄÜĮ÷¶Æ 0”ęŅŌĻĀ£¬Ė®·Ö×Ó²»ŌŁŌĖ¶Æ | |
| D£® | 50mLĖ®ŗĶ50mL¾Ę¾«»ģŗĻŗóµÄ×ÜĢå»żŠ”ÓŚ100mL ·Ö×ÓµÄÖŹĮæŗĶĢå»ż¶¼ŗÜŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŖĮĖÉķĢ彔浣¬±ŲŠė¾łŗāÉÅŹ³ | |
| B£® | ĪŖŌ¤·ĄČ±µāŠŌ¼²²”£¬æÉŹ³ÓĆŹŹĮæŗ£“ų | |
| C£® | ĪŖŹ¹·¢ĆęŹ³Ę·ĖÉČķæÉæŚ£¬ÖĘ×÷Ź±æÉĢķ¼ÓŹŹĮæĢ¼ĖįĒāÄĘ | |
| D£® | ĪŖŃÓ³¤Ź³Ę·±£ÖŹĘŚ£¬ŌŚŹ³Ę·ÖŠĢķ¼Ó“óĮæ·ĄøƼĮ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŹµŃé ²½Öč |  | 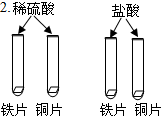 | 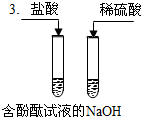 |
| ŹµŃé ĻÖĻó | ČÜŅŗ±äĪŖ ŗģÉ« | Ļ”ĖįÖŠµÄĢśĘ¬±ķĆę¶¼ÓŠ ĘųÅŻ²śÉś£¬Ķʬ±ķĆę¶¼Ć»ÓŠĆ÷ĻŌĻÖĻó | ČÜŅŗÓÉŗģÉ«±äĪŖ ĪŽÉ« |
| ·ÖĪö Óė ½įĀŪ | ½įĀŪ£ŗĻ”ĖįÄÜÓėÖøŹ¾¼Į×÷ÓĆ | ĢśÓėĻ”ĮņĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖFe+H2SO4ØTFeSO4+H2”ü ½įĀŪ£ŗĻ”ĖįÄÜÓė»īĘĆ½šŹō·“Ó¦ | ½įĀŪ£ŗ ĖįÄÜŗĶ¼ī·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

| ””ĪļÖŹ | ””NaCl | ””NH4CO3 | ””NH4Cl | ””NaHCO3 |
| ””Čܽā¶Č | ””36.0 | ””21.6 | ””37.2 | ””9.6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
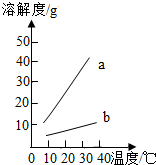 ČēĶ¼ĖłŹ¾ŹĒNa2CO3ŗĶNaHCO3µÄČܽā¶Č±ķ¼°Čܽā¶ČĒśĻߣ®øł¾ŻĶ¼±ķ»Ų“šĻĀĮŠĪŹĢā£ŗ
ČēĶ¼ĖłŹ¾ŹĒNa2CO3ŗĶNaHCO3µÄČܽā¶Č±ķ¼°Čܽā¶ČĒśĻߣ®øł¾ŻĶ¼±ķ»Ų“šĻĀĮŠĪŹĢā£ŗ| 10”ę | 20”ę | 30”ę | 40”ę | |
| Ģ¼ĖįÄĘ/g | 12.5 | 21.5 | 39.7 | 49.0 |
| Ģ¼ĖįĒāÄĘ/g | 8.1 | 9.6 | 11.1 | 12.7 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com