
| A. | +1 | B. | +2 | C. | +5 | D. | +7 |
科目:初中化学 来源: 题型:推断题
 请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站,“2-5号站”各站的对应物质属于不同类别的纯净物.
请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站,“2-5号站”各站的对应物质属于不同类别的纯净物.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
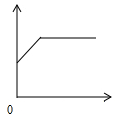 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )| 选项 | 实验操作 | 横坐标 | 纵坐标 |
| A | 向一定质量的锌粉中加入稀硫酸 | 加入稀硫酸的质量/g | 生成氢气的质量/g |
| B | 向一定质量的硝酸银溶液中加入铜粉 | 加入铜粉的质量/g | 溶液的质量/g |
| C | 向一定质量的稀盐酸中不断加入碳酸钙粉末 | 加入碳酸钙的质量/g | 溶液的质量/g |
| D | 向氯化钠饱和溶液中加入水 | 加入水的质量/g | 溶质的质量/g |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com