我们知道氧气是人体生命所必需的,在一般情况下,人可以呼吸空气中的氧气,但在特殊情况下,如在核潜艇里工作的人员,如何获得氧气呢?研究表明用“金属过氧化物处理系统”使氧“再生”具有良好的实际应用价值.
已知:淡黄色的过氧化钠固体在常温下即能与二氧化碳反应生成氧气反应方程式为:2Na
2O
2+2CO
2═2Na
2CO
3+O
2(1)你认为用这种方法制氧气的优点是
反应条件低、方便携带、产物无污染、产生氧气同时还吸收了二氧化碳
反应条件低、方便携带、产物无污染、产生氧气同时还吸收了二氧化碳
.
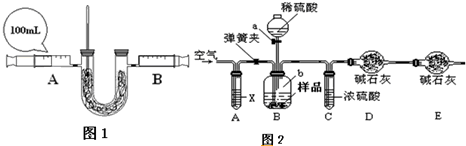
(2)小明欲探究过氧化钠吸收和释放的气体之间体积关系以及反应的热效应,设计实验如图1,请回答下列相关问题:
①检查装置气密性.
②向U形管内盛装过量的Na
2O
2药品,注射器中为二氧化碳气体,连接好装置.
③缓缓推动注射器A活塞,片刻,可以观察到温度计液柱明显上升,说明反应放热,同时还可以观察到固体粉末发生变化的现象是
淡黄色的粉末逐渐变为白色粉末
淡黄色的粉末逐渐变为白色粉末
;
④小明查阅资料得知:相同的条件下,相同体积的气体具有相等的分子数,则待A注射器中二氧化碳气体反应完全后,装置恢复至常温,B注射器中活塞应停留在
50
50
mL处.(不考虑实验带来的误差)
(3)Na
2O
2露置在空气中容易发生变质,如何检验已经变质?简述方法、现象和结论.
取少量固体样品滴加稀盐酸,将产生的气体通入澄清石灰水若出现浑浊说明已变质
取少量固体样品滴加稀盐酸,将产生的气体通入澄清石灰水若出现浑浊说明已变质
.
变质的程度如何呢?部分同学对“已部分变质的Na
2O
2(含Na
2CO
3)的纯度测定”设计了实验,已知Na
2O
2与稀硫酸不反应,碱石灰能吸收CO
2和H
2O,步骤如下:
①按图2连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为w
1g;
③准确称得mg样品放入容器b中;
④打开a,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为w
2g;
⑥根据D装置质量差进行计算.
试回答:
(i)若④⑤两步的实验操作太快,则会导致测定的Na
2O
2的纯度
偏大
偏大
(填“偏大”或“偏小”).
(ii)鼓入空气的目的是
将装置中残留的二氧化碳鼓出,使反应充分
将装置中残留的二氧化碳鼓出,使反应充分
,装置A中试剂X应选用
NaOH溶液
NaOH溶液
;
(iii)E装置的作用是
防止空气中的二氧化碳和水蒸气进入D装置
防止空气中的二氧化碳和水蒸气进入D装置
.

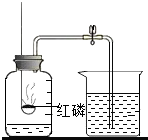 人类每时每刻都离不开空气,没有空气就没有生命,也就没有生机勃勃的地球.
人类每时每刻都离不开空气,没有空气就没有生命,也就没有生机勃勃的地球.
