
| A. | 溶液中溶质一定都是固体的 | |
| B. | 溶液都是均一、稳定、无色透明的混合物 | |
| C. | 某温度下,在食盐的饱和溶液中不能再溶解任何溶质 | |
| D. | 某温度下,从一瓶蔗糖的饱和溶液中取出一部分,则剩余溶液仍是蔗糖的饱和溶液 |
分析 A、根据溶质的状态,进行分析判断.
B、根据溶液的特征,进行分析判断.
C、根据饱和溶液的特征,进行分析判断.
D、根据溶液具有均一性,进行分析判断.
解答 解:A、溶液中溶质不一定都是固体,也可能是液体或气体,故选项说法错误.
B、溶液都是均一、稳定、透明的混合物,但不一定是无色的,如硫酸铜溶液显蓝色,故选项说法错误.
C、某温度下,在食盐的饱和溶液中还能溶解其它的溶质,故选项说法错误.
D、溶液具有均一性,某温度下,从一瓶蔗糖的饱和溶液中取出一部分,则剩余溶液仍是蔗糖的饱和溶液,故选项说法正确.
故选:D.
点评 本题难度不大,掌握饱和溶液的特征、溶液的特征并能灵活运用是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
 钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注,常温下Ti不和非金属、强酸反应,红热时,却可与许多非金属单质反应,钛是航空、宇航、军工、电力等方面的必需原料.地壳中含钛矿石之一,称金红石(TiO2),目前大规模生产钛的方法是:首先将金红石、炭粉混合在高温条件下通入氯气制得TiCl4和一种可燃性气体,该步反应的化学方程式是TiO2+2C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.第二是在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应,制得金属钛.此反应的化学方程式为2Mg+TiCl4$\frac{\underline{\;氩气\;}}{△}$2MgCl2+Ti.
钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注,常温下Ti不和非金属、强酸反应,红热时,却可与许多非金属单质反应,钛是航空、宇航、军工、电力等方面的必需原料.地壳中含钛矿石之一,称金红石(TiO2),目前大规模生产钛的方法是:首先将金红石、炭粉混合在高温条件下通入氯气制得TiCl4和一种可燃性气体,该步反应的化学方程式是TiO2+2C+2Cl2$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO.第二是在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应,制得金属钛.此反应的化学方程式为2Mg+TiCl4$\frac{\underline{\;氩气\;}}{△}$2MgCl2+Ti.查看答案和解析>>
科目:初中化学 来源:江苏省无锡市长泾片2017届九年级下学期第二次模拟考试化学试卷 题型:选择填充题
如图是A、B、C三种物质的溶解度曲线,下列说法不正确的是
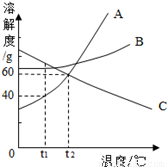
A. t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A
B. 当A中含有少量B时,可以通过冷却热饱和溶液的方法提纯A
C. t2℃时,A和C的饱和溶液中含有相同质量的溶质
D. 将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是B>C>A
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
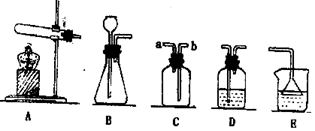
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | M | N | Q | P |
| 反应前质量(g) | 18 | 1 | 2 | 32 |
| 反应后质量(g) | X | 26 | 2 | 12 |
| A. | 该变化的基本反应类型是分解反应 | B. | 反应后物质X的值为l3 | ||
| C. | 反应中N、P的质量比为5:4 | D. | 物质Q可能是该反应的催化剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com