
【题目】某化学兴趣小组借助U型玻璃管粗略测定空气中氧气的体积分数约为1/5,实验装置如图所示,下列说法不正确的是
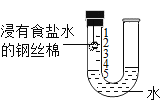
A.钢丝棉的用量不影响实验结果
B.食盐水加快了钢丝棉的锈蚀
C.观察到U型玻璃管左边液面上升,右边液面下降
D.实验前要检查装置气密性
【答案】A
【解析】
A、为保证U型玻璃管左管氧气被充分反应,加入的钢丝棉量要足量,此选项错误;
B、钢丝棉在食盐水的环境下,加快了锈蚀,此选项正确;
C、钢丝棉生锈消耗空气中的氧气,使U型玻璃管左边内部压强变小,在实验装置气密性良好的情况下,外界的大气压大于左边内部压强,导致右边的水面下降,左边的液面上升,此选项正确;
D、本题借助U型玻璃管粗略测定空气中氧气的体积分数,原理是利用钢丝棉生锈消耗空气中的氧气,使U型玻璃管左边内部压强变小,在实验装置气密性良好的情况下,外界的大气压大于左边内部压强,导致右边的水面下降,左边的液面上升,为保证实验结果准确,实验前要检查装置气密性,此选项正确。
故选A。


科目:初中化学 来源: 题型:
【题目】将NaOH和NH4NO3固体分别装入两支试管中,进行如图一所示实验,向两支试管中分别滴加适量水,烧杯中X、Y的饱和溶液均变浑浊。请结合图二回答:
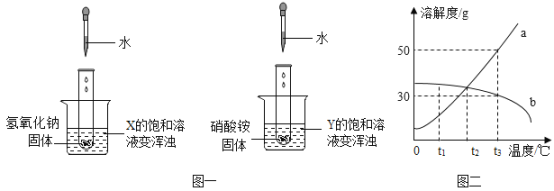
(1)X的溶解度曲线为_____(填“a”或“b”)。
(2)将t3℃时等质量的X、Y饱和溶液降温到t2℃,所得溶液的质量:X____Y(选填“>”、“=”或“<”)。
(3)t3℃时,将90gY的饱和溶液稀释为溶质质量分数为20%的溶液,需加水的质量为____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】芯片的核心材料是高纯硅,下图是利用石英砂(主要成分SiO2)制取高纯硅的流程图,请回 答下列问题:
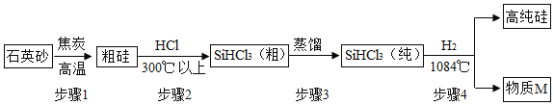
(1)SiO2与金刚石结构相似,则构成SiO2的粒子是__(填“分子”、“原子”或“离子”)。
(2)步骤 1 发生的反应为:SiO2+ 2C![]() Si + 2X↑,上述反应中 X 是______(填化学式),其中SiO2发生了______(填“氧化”或“还原”)反应。
Si + 2X↑,上述反应中 X 是______(填化学式),其中SiO2发生了______(填“氧化”或“还原”)反应。
(3)步骤 3 中“蒸馏”属于__(填“物理”或“化学”)变化。
(4)步骤 4 中物质 M 在该生产过程中可循环使用,写出步骤 4 反应的化学方程式:______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一种在古籍里称为“鋈”的银白色铜合金,是古代云南、四川地区的特产,其主要成分是铜、锌、镍等金属单质,炼制时需要黑铜矿(主要成分是CuO)、硫化镍矿(主要成分是Ni2S3)等多种矿物。下列有关说法不正确的是
A.鋈属于金属材料
B.鋈的样品在足量稀盐酸中能全部溶解
C.Ni2S3中镍元素呈+3价
D.黑铜矿跟木炭共热能生成单质铜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】食盐是一种重要的化工原料。请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤。
![]()
①操作I所用的玻璃仪器有:烧杯、玻璃棒和_______。
②在蒸发过程中,待_________时,停止加热,利用余热将滤液蒸干。
(2)为了除去NaCl溶液中含有少量的MgCl2、CaCl2和Na2SO4等杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定的顺序进行如下图所示的实验:

回答下列问题:
①实验I中加入试剂A除去的杂质是_______;
②实验Ⅱ中加入的试剂B是________溶液;
③滤液②中除Na+和Cl-外,还含有的离子是_______(填离子符号);
④实验Ⅲ中发生的中和反应的化学方程式为_________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室常利用以下装置完成气体制备及性质实验。请回答:
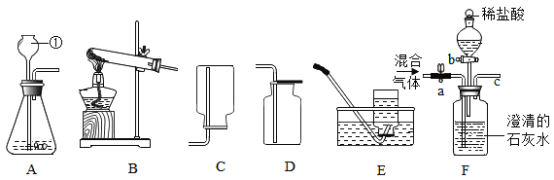
(1)写出图中标号①的仪器名称:_________________。
(2)欲使用高锰酸钾制取氧气,应选择的发生装置是________________(填标号),写出反应化学方程式_________________。若使用E装置收集氧气,实验结束时,应先从水槽中移出导气管,再熄灭酒精灯,原因是_________________。
(3)将CO2和CO的混合气体通过F装置(液体药品均足量)
①实验开始时关闭活塞b,打开活塞a,广口瓶中观察到的现象是_________________。
②待充分反应后,再关闭活塞a,打开活塞b,将分液漏斗中的稀盐酸滴入广口瓶中,一段时间后,用燃着的木条放c处发现木条熄灭,则此时逸出的气体主要成分是_________________, 写出 该反应的化学方程式_________________,欲收集该气体,最适合选择的装置是________________(填标号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某探究小组选用如图所示部分装置测量一定量的高锰酸钾分解产生的氧气的体积,请回答有关问题:

(1)写出图中标号仪器的名称:②_____。
(2)该实验中产生氧气反应的表达式为_____(写文字表达式或符号表达式均可)。该小组制取氧气并测量产生氧气的体积,导管的连接顺序是_____ (填序号),实验中水被染红,可能的原因是_____。实验结束后他们发现收集到气体的体积比计算出来的理论值偏少,原因可能是_____(写一点)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小峰同学在体育课上腿部擦伤,医务室的大夫在他伤口上涂了医用过氧化氢溶液,小峰看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
I.小峰准备用如图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。

(1)请写出过氧化氢分解的文字表达式:_____。
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到_____,说明生成的气体是氧气。
Ⅱ.小峰查阅了相关资料,并进行了探究实验
(查阅资料)
(1)过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
(2)温度对化学反应的快慢有影响,人体正常体温是37℃。
(提出猜想)
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
(进行实验)
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 分两次进行实验,均注入5mL过氧化氢溶液第一次在常温下进行第二次将试管浸在37℃的温水中 | 量筒中2分钟收集到的气体体积均为6mL | _____ |
② | 分两次进行实验 第一次,量筒中2分钟收 第一次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液 第二次_____ | 第一次,量筒中2分钟收集到的气体体积为56mL 第二次,量筒2分钟收 集到的气体体积为6mL | 过氧化氢分解加快是因过氧氢酶的作用 |
(3)序号①实验得出的实验结论是:猜想1_____(成立或不成立)
(4)序号②实验第一次实验中2分钟生成的氧气体积为_____mL。
(5)序号②实验中第二次实验(横线部分)应进行的操作是_____。
(实验结果)
小峰通过实验,认为是因为过氧化氢酶的存在能加快过氧化氢分解。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知 CuS、Cu2S 粉末的颜色和 CuO 相似,且都不溶解于水。在空气中煅烧时,CuS 和Cu2S 都转化成 CuO 和 SO2。
(1)请写出 CuS、Cu2S 在空气中煅烧时发生反应的化学方程式:________、________。
(2)根据叙述,设计一个不用其他化学试剂鉴别 CuO、CuS、Cu2S三种粉末的实验方案(写明步骤与结论)________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com