
 如图是 A、B、C三种物质的溶解度曲线,回答下列问题:
如图是 A、B、C三种物质的溶解度曲线,回答下列问题: ×100%,t3℃时A、B、C三种物质饱和溶液的溶质质量分数与溶解度成正比,所以:A>B>C,降低温度后,A和B都会析出晶体,仍是饱和溶液;因为在t1℃时B的溶解度大于A,所以溶质质量分数是B>A,但是C降低温度后成为不饱和溶液,溶质质量分数不变,所以溶质质量分数由小到大的顺序为:C<A<B;
×100%,t3℃时A、B、C三种物质饱和溶液的溶质质量分数与溶解度成正比,所以:A>B>C,降低温度后,A和B都会析出晶体,仍是饱和溶液;因为在t1℃时B的溶解度大于A,所以溶质质量分数是B>A,但是C降低温度后成为不饱和溶液,溶质质量分数不变,所以溶质质量分数由小到大的顺序为:C<A<B;

科目:初中化学 来源: 题型:
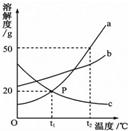 33、如图是a、b、c三种固体物质的溶解度曲线.
33、如图是a、b、c三种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:
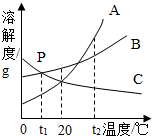 (2012?大田县质检)如图是A、B、C三种固体物质的溶解度曲线图,请回答:
(2012?大田县质检)如图是A、B、C三种固体物质的溶解度曲线图,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:
 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com