
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
| 反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 3.5 |
| 剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 | 2.04 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 1.取烧杯M中的少量溶液于试管A中,向其中加入一定量的稀盐酸 | 溶液由红色变为无色且有气泡产生. | 小红 的猜想不正确 |
| 2.另取烧杯M中的少量溶液于另一试管B中,向其中加入过量氯化钡溶液. | 出现白色沉淀 | 小亮的猜想正确 |
| 3.继续向试管B中加入过量的稀盐酸 | 沉淀一部分消失,并生成气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
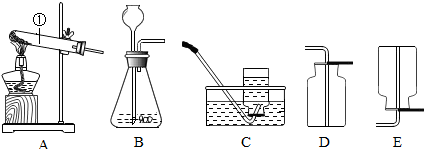
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化学反应前后分子的总数可能会发生变化 | |
| B. | 燃烧都伴随着发光、放热,所以有发光、放热现象的一定是燃烧 | |
| C. | 化合物至少由两种元素组成,所以由两种元素组成的物质一定是化合物 | |
| D. | 用水灭火的原理是降低了可燃物的着火点 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用pH计测定溶液的pH | B. | 用体温计测最沸水的温度 | ||
| C. | 用交流电源进行电解水实验 | D. | 用刻度尺直接测量分子的直径 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 反应时间(秒) | 0 | 25 | 50 | 75 | 100 | 125 | 150 | 175 | 200 |
| 滴入稀盐酸体积(毫升) | 0 | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 |
| pH | 13.2 | 13.0 | 12.7 | 12.4 | 12.1 | 7.0 | 2.0 | 1.6 | 1.3 |
| 温度(℃) | 36.9 | 37.5 | 38.0 | 38.5 | 38.8 | 39.2 | 39.0 | 38.8 | 38.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com