
【题目】下列装置常用于实验室制取气体.根据给出的装置回答下列问题
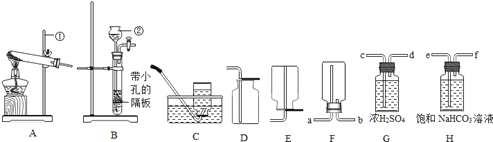
(1)指出编号仪器名称:②________.
(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为_________________.
(3)制取并收集二氧化碳应选择的装置是________(从A——E中选择),使用该套装置制取气体的突出优点是___________________________________,该反应原理用化学方程式表示为_________________改用F装置收集二氧化碳,则气体应从_________端进入.制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使个G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→______________(用端口字母表示).
(4)将纯净的二氧化碳气体通入盛有蒸馏水的洗气瓶一段时间后,测得该装置中溶液的pH____ (填“>”、“<”或“=”)7.
【答案】长颈漏斗 ![]() B、E 可以随时使反应进行,也可以随时使反应停止 CaCO3+2HCl=CaCl2+H2O+CO2↑ b e→f→c→d <
B、E 可以随时使反应进行,也可以随时使反应停止 CaCO3+2HCl=CaCl2+H2O+CO2↑ b e→f→c→d <
【解析】
(1)②是长颈漏斗.
(2)实验室可以用加热高锰酸钾的方法制取氧气,高锰酸钾受热时分解能生成锰酸钾、二氧化锰和氧气,反应的化学方程式为![]() 。
。
(3)制取二氧化碳可以用B装置,二氧化碳的密度比空气大,可以用向上排空气法收集,用E装置.故填:B、E。
使用该套装置制取气体的突出优点是:可以随时使反应进行,也可以随时使反应停止.
实验室用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石或石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应能生成氯化钙、水和二氧化碳,化学方程式为:
CaCO3+2HCl=CaCl2+H2O+CO2↑.
用F装置收集二氧化碳时,气体应从b端进入.
要除去氯化氢气体与水蒸气,应该先除去氯化氢,再除去水,连接顺序为:混合气体→e→f→c→d.
(4)二氧化碳和水反应生成碳酸,碳酸显酸性,pH小于7.


科目:初中化学 来源: 题型:
【题目】为保护哈市的空气质量,降低汽车尾气的污染,哈市再次推出了气电混合动力公交车。目前,哈市电车公司101、102、103路公交线路的80台气电混合动力公交车齐上道。 混合动力公交车节油和节气,时速23公里内“静音”不烧气,减少尾气的排放。请回答下列问题:

(1) 该公交汽车车体外表的铁质外壳喷涂一层黄色漆,其目的是___________。
(2)该公交车在时速低于23公里行驶时,此过程中的能量转化是(用“―”表示转化)___________________。
(3) 该公交车的轮胎中的材料含有合成橡胶、炭黑和钢丝,该材料为_______(填字母)。
A.金属材料 B.复合材料 C.合成材料
(4) 在生活生产中,人们经常利用的能源有①______________________________等;随着科学技术的发展,人们正在利用开发其他新能源如太阳能等,新能源的使用的意义②______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】完成下列化学方程式
(1)碳在空气中燃烧__________。
(2)碳酸氢钠与稀盐酸反应__________。
(3)氢氧化钠与稀硫酸反应__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两物质的溶解度曲线如图所示,下列叙述正确的是
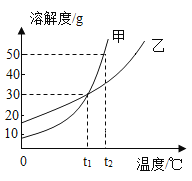
A.t1℃时,甲、乙各30g分别加入70g水中均恰好饱和
B.t1℃时,甲、乙两物质形成的溶液溶质的质量分数相等
C.t2℃时,在l00g水中放入100g甲,所得溶液溶质的质量分数为50%
D.t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水和溶液与生活、生产密切相关。请回答:
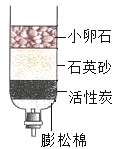
(1)用如图所示的简易装置净化水时,其中活性炭的主要作用是_____。
(2)硬水中含有较多的_____(填序号)。
①碳酸钙 ②氢氧化镁 ③可溶性钙、镁化合物
(3)实验室中,常采用_____的方法来降低水的硬度。
(4)甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如下:
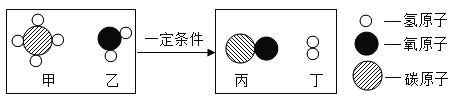
由图可知,水煤气的成分是_____(填化学式),反应后生成物丙和丁的分子个数比为_____。
(5)下列说法不正确的是_____。
A 硝酸铵固体溶于水,会出现放热现象
B 洗洁精可乳化餐具上的油污
C 铁锈可用稀盐酸浸泡除去
D 冷却热的饱和溶液的方法可以使硝酸钾晶体析出
(6)以粗盐(含杂质Na2SO4、MgCl2、CaCl2、泥沙)为原料制备精盐并配制溶液。
Ⅰ.加水溶解后,用如图装置除去粗盐中的泥沙,玻璃棒的作用是_____。
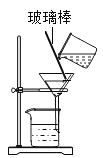
Ⅱ.为除去Na2SO4、MgCl2、CaCl2,并得到中性的食盐溶液,下列所加试剂和操作:①加过量的Na2CO3溶液,②过滤,③加过量的NaOH溶液,④加适量的稀盐酸,⑤加过量的BaCl2溶液,能达到目的的顺序是_____。
A ⑤③②①④
B ③⑤①④②
C ③⑤①②④
Ⅲ.用pH试纸检验溶液是否呈中性的操作:_____。
Ⅳ.如图为氢氧化钠与盐酸反应的示意图,从反应前后离子的种类看,有些离子参与了反应,有些离子只是旁观者,该反应中参与反应的离子是_____。
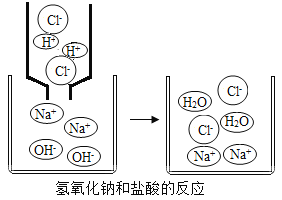
Ⅴ.2018年南京市中考化学实验操作考查项目之一:用固体氯化钠和水配制50g质量分数为6%的氯化钠溶液。其主要步骤是计算、称量、量取、_____、装瓶贴标签。在实际操作中某同学量取水时,仰视读数,会导致所配制的溶液的质量分数_____(填:“偏大”或“偏小”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学用语是学习化学的工具,下列化学用语表述不正确的是( )
A.过氧化氢中氢、氧元素的化合价:![]()
B.氯离子的结构示意图: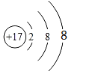
C.工业炼铁的主要反应原理: 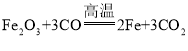
D.淀粉的化学式:C6H10O5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是A、B、C三种固体的溶解度曲线,请据图回答下列问题:
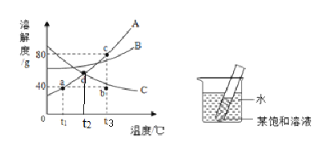
(1)d点所表示的意义是_______,t1°C时,A、B、C三种物质的溶解度大小顺序为_____
(2)t3°C时,30gA物质加入到50 g水中不断搅拌,所得溶液溶质质量分数为_____(保留到0.1%)
(3)t3℃时,相同质量的A、B、C三种物质的饱和溶液降温至t1°C,析出晶体最多的是_____,此时三种物质的溶液的溶质质量分数由大到小的顺序是________。
(4)如图所示,试管内装有A、B、C三种物质之一的饱和溶液,向烧杯中的水中加入氢氧化钠固体,试管中有晶体析出。由此判断试管内的溶液是________(填字母序号)物质的溶液。
(5)某同学在实验室用固体B和蒸馏水配制50 g质量分数为6%的B溶液时,涉及以下实验步骤:① 溶解② 称量和量取③ 计算④ 装入试剂瓶贴好标签。配制上述溶液正确的实验步骤顺序是____________(填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一固体混合物A,该混合物中可能含有BaCl2、Na2CO3、NaCl、CuCl2四种物质中的两种或多种.按如图所示进行实验,出现的线性如图所述(假设过程中所有可能发生的反应恰好都完全进行).
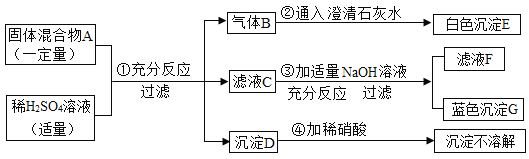
试根据实验过程和发生的现象做出判断,填写下列空白:
(1)沉淀D的化学式为_____;气体R的化学式为_____.
(2)滤液F中的溶质为_____.
(3)混合物A中不能确定含有的物质是_____.
(4)写出①汇总所发生反应的化学方程式:_____;_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纳米材料具有特殊的性质和功能。纳米二氧化钛(TiO2)具有很高的化学稳定性、热稳定性,能参与的光催化反应,可使吸附在其表面的甲醛等物质被氧化。正钛酸(H4TiO4)在一定条件下分解失水可制得纳米TiO2。下列说法不正确的是
A.甲醛对人体健康有害
B.纳米TiO2添加到墙面涂料中,有利于消除甲醛
C.纳米二氧化钛受热易分解
D.制备纳米TiO2的反应为H4TiO4 TiO2+2H2O
TiO2+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com