
分析 镁比铝活泼,铝比铁活泼,铁比银活泼;
铁和稀盐酸或稀硫酸反应生成氯化亚铁或硫酸亚铁和氢气;
根据反应的化学方程式和反应物、生成物之间的质量关系可以进行相关方面的计算.
解答 解:(1)滤渣中一定含有反应生成的银,发现滤液中含有二价铁离子,说明镁和铝已经完全反应,因此一定没有镁和铝,可能含有过量的铁;
为了进一步证明可能含有的物质是否存在,实验中需向滤渣中加入的试剂是稀盐酸或稀硫酸,因为铁和稀盐酸或稀硫酸反应生成氯化亚铁或硫酸亚铁和氢气.
故填:银;镁和铝;铁;稀盐酸或稀硫酸.
(2)滤液中一定含有的金属阳离子有Mg2+、Al3+、Fe2+.
故填:Mg2+、Al3+、Fe2+.
(3)由2Al+2NaOH+2H2O═2NaAlO2+3H2↑和2Al+3H2SO4═Al2(SO4)3+3H2↑可知,如果质量相同的铝分别与足量的氢氧化钠溶液,稀硫酸溶液充分反应后.产生气体的质量之比是1:1.
故填:1:1.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.


科目:初中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 各取2mL反应后的混合溶液分别加入A、B两只试管 | / |
| 2 | 向A试管中滴加足量的稀硫酸,随即滴入几滴红色品红溶液 | 产生气泡,品红溶液褪色.证明含有K2SO3 |
| 3 | 向B试管中,加入足量氯化钡溶液,再加入足量的稀盐酸 | 先有白色沉淀,后有气体产生,沉淀部分溶解,证明含有 K2SO4,则猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 石墨烯是一种新型的碳单质 | |
| B. | 四种物质中的碳原子排列方式相同 | |
| C. | 四种物质完全燃烧后的产物都是CO2 | |
| D. | 将石墨变成石墨烯发生了化学变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )
液化石油气中含有丙烷,关于丙烷的下列叙述正确的是( )| A. | 丙烷是由3个碳原子和8个氢原子构成的 | |
| B. | 丙烷中碳、氢元素的质量比为3:8 | |
| C. | 一个丙烷分子中有26个电子 | |
| D. | 丙烷属于无机化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 了解水、保护水是每个公民的义务和责任.请回答:
了解水、保护水是每个公民的义务和责任.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
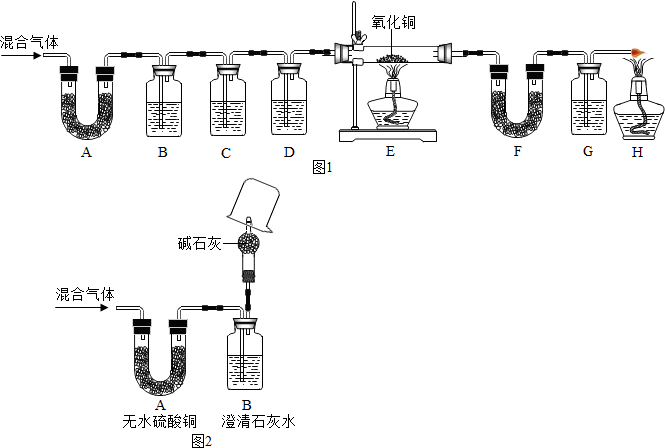
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
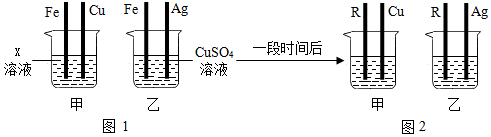
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com