
| A. | H+和Cu2+来自同一工厂 | B. | Cu2+和K+来自同一工厂 | ||
| C. | H+和OH-来自同一工厂 | D. | OH-和Cu2-来自同一工厂 |
分析 利用离子的共存来判断两厂废水的成分,因0H-与H+、Cu2+不能共存,且每个工厂的生产污水中各含有下列五种离子中的三种,则含H+、Cu2+的污水中的阴离子为NO3-,即其中一个厂污水中的离子为:H+、Cu2+、NO3-;则另一厂污水中离子为K+、NO3-、0H-;据此分析.
解答 解:因0H-与H+、Cu2+不能共存,且每个工厂的生产污水中各含有下列五种离子中的三种,则含H+、Cu2+的污水中的阴离子为NO3-,即其中一个厂污水中的离子为:H+、Cu2+、NO3-;则另一厂污水中离子为K+、NO3-、0H-;
A、根据分析其中一厂污水中有H+、Cu2+、NO3-;故正确;
B、根据离子的共存及两厂污水中各含三种离子,两厂污水中的离子分别为:H+、Cu2+、NO3-;K+、NO3-、0H-,可知Cu2+、K+不来自同一工厂,故错误;
C、因OH-和H+能结合生成水,则不能来自同一工厂,故错误;
D、因OH-和Cu2+能结合生成沉淀,则不能来自同一工厂,故错误;
故选A.
点评 本题考查利用复分解反应的条件及溶液不显电性来判断工厂污水中的离子,具有较强的实际应用性,要求学生能将所学知识进行迁移应用,注意与习题信息结合及思维的严密性.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
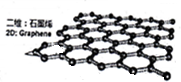 碳及其化合物在生产、生活中应用广泛.
碳及其化合物在生产、生活中应用广泛.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
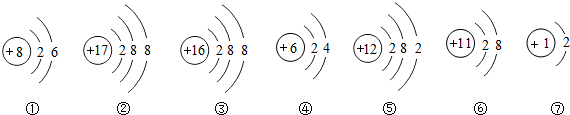
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验某气体是否为CO2 | 将燃着的木条伸入气体中 |
| B | 鉴别NaCl溶液和稀盐酸 | 滴加无色酚酞溶液 |
| C | 除去CaCO3中的Na2CO3 | 加水溶解,过滤 |
| D | 除去CO2中的CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
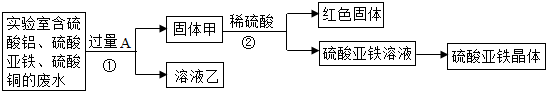
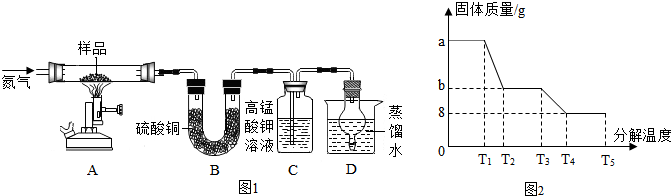
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com