
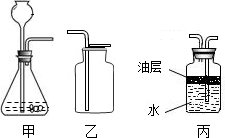
 (2013?温州)小明和小红利用右图装置,以碳酸钙和稀盐酸为原料来制取二氧化碳气体,并进行比较分析.
(2013?温州)小明和小红利用右图装置,以碳酸钙和稀盐酸为原料来制取二氧化碳气体,并进行比较分析.

科目:初中化学 来源: 题型:
(2013?温州)根据物质的组成.小明将部分物质分为甲、乙两类(如表所示).下列对分类结果判断正确的是( )
|
查看答案和解析>>
科目:初中化学 来源: 题型:
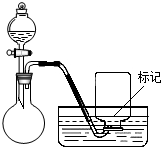 (2013?温州)气体的密度容易受温度和压强的影响.为了测量常温常压下氧气的密度,在老师的指导下,小明进行了如下实验:
(2013?温州)气体的密度容易受温度和压强的影响.为了测量常温常压下氧气的密度,在老师的指导下,小明进行了如下实验:| m1-m2 |
| 10V0 |
| m1-m2 |
| 10V0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验操作 | 设计要求 |
| 步骤一:取3支洁净的试管标为A、B、C,在各试管中分别加入1%淀粉溶液2毫升;向A 试管加入l 毫升稀盐酸和l 毫升唾液;向B试管加入1毫升氢氧化钠溶液和1毫升唾液;向C试管加入 l毫升蒸馏水和1毫升唾液 l毫升蒸馏水和1毫升唾液 |
设置对照实验 |
| 步骤二: 同时将三支试管放入盛有37℃的水中,恒温水浴 同时将三支试管放入盛有37℃的水中,恒温水浴 |
控制实验条件 |
| 步骤三:10分钟后,往3支试管中分别滴入1滴碘液,观察颜色变化. | 获取实验证据 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?温州)小明在老师的指导下测一瓶稀盐酸的溶质质量分数,具体步骤如下:
(2013?温州)小明在老师的指导下测一瓶稀盐酸的溶质质量分数,具体步骤如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com