
������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߡ�
��1��Na2CO3�ܽ������Ϊ�� ����a��b����
| | 0�� | 10�� | 20�� | 30�� | 40�� |
| Na2CO3���ܽ�ȣ�g/100gˮ�� | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3���ܽ�ȣ�g/100gˮ�� | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
��2��Ҫ��ȥNaHCO3�����е�����Na2CO3��Ӧ���õ������������� ����д��ţ���
��. ��ȴ�ᾧ�� ��. �����ᾧ�� ��. �ܽ����
��3����֪Na2CO3ת��ΪNaHCO3�ķ�ӦΪNa2CO3+CO2+H2O��2NaHCO3,����������Ϣ��Ҫ��ȥNaHCO3������Һ�е�����Na2CO3��Ӧ���õĻ�ѧ�������� ��������������
��4��40��ʱ��100.0g Na2CO3�ı�����Һ�к��������� g���ʣ�����Һ��������������Ϊ������ %�����Ƹ���Һ��Ҫ���� gʯ��������� mLˮ������������ȷ��0.1��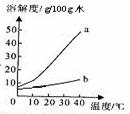
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
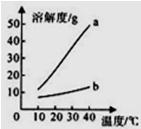
 6��������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�
6��������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�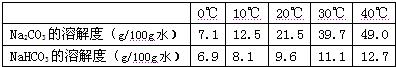
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
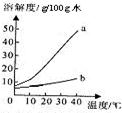
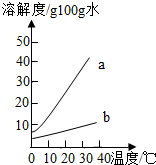 ������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�
������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�| 0�� | 10�� | 20�� | 30�� | 40�� | |
| Na2CO3���ܽ�ȣ�g/100gˮ�� | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3���ܽ�ȣ�g/100gˮ�� | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
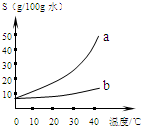 ������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�
������Na2CO3��NaHCO3���ܽ�ȱ����ܽ�����ߣ�| 0�� | 10�� | 20�� | 30�� | 40�� | |
| Na2CO3���ܽ�ȣ�g/100gˮ�� | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3���ܽ�ȣ�g/100gˮ�� | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ͬ���� ���ͣ������

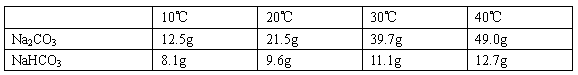
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com