
 化学小组同学在帮实验员整理药品时,发现一瓶标签残缺的无色溶液(如图1所示),为确定其中溶质的成分,进行了如下探究活动.
化学小组同学在帮实验员整理药品时,发现一瓶标签残缺的无色溶液(如图1所示),为确定其中溶质的成分,进行了如下探究活动. | 物质 | NaOH | NaCl | Na2SO4 | NaNO3 | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 109 | 36 | 19.5 | 87 | 21.5 | 9.6 |
| 水溶液的酸碱性 | 碱性 | 中性 | 中性 | 中性 | 碱性 | 碱性 |
| 实验操作 | 测定结果或现象 | 得出结论 |
| 取少量待测液于试管中,测溶液的pH | pH>7 | 溶质不可能是氯化钠、硫酸钠、硝酸钠 |
| 取少量待测液于试管中,加入2mL稀盐酸 | 观察到产生气泡 | 溶质是碳酸钠 |
分析 【分析讨论】
饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
【实验探究】
显酸性溶液pH小于7,显碱性溶液pH大于7,显中性溶液pH等于7;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
【反思交流】
氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水;
【进一步探究】
碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,显碱性溶液能使酚酞试液变红色;
【总结提高】
倾倒液体药品时,为防止标签损坏,标签应该向着手心,且药品取用完毕后应及时盖好瓶塞.
解答 解:【分析讨论】
室温时饱和碳酸氢钠溶液质量分数为:$\frac{9.6g}{100g+9.6g}$×100%=8.8%,因此溶液中的溶质不可能是NaHCO3.
故填:室温时碳酸氢钠饱和溶液的质量分数小于15%.
【实验探究】
取少量待测液于试管中,测溶液的pH小于7,溶质不可能是氯化钠、硫酸钠、硝酸钠,取少量待测液于试管中,加入2mL稀盐酸产生气泡,溶质的碳酸钠,实验过程如下表所示:
| 实验操作 | 测定结果或现象 | 得出结论 |
| 取少量待测液于试管中,测溶液的pH | pH>7 | 溶质不可能是氯化钠、硫酸钠、硝酸钠 |
| 取少量待测液于试管中,加入2mL稀盐酸 | 观察到产生气泡 | 溶质是碳酸钠 |
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:初中化学 来源: 题型:选择题
| A. | 地球上的水资源非常丰富,但是可供利用的淡水资源是很有限的 | |
| B. | 石油分馏可得到汽油、煤油、柴油等,此过程石油发生了分解反应 | |
| C. | pH<5.6的酸性降水称为酸雨,它的形成与大气中SO2等污染物有关 | |
| D. | 使燃料充分燃烧,既可以减少空气污染,又可以节约化石能源 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
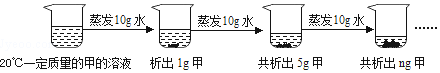
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 成分 | 水 | 蛋白质 | 脂肪 | 糖类 | 钙 | 磷 | 铁 | 维生素 |
| 平混含量(%) | 96.0 | 1.8 | 0.7 | 1.1 | 0.01 | 0.03 | 0.0005 | 0.015 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 长期放置后不会分层的液体一定是溶液 | |
| B. | 在沉淀、吸附、过滤、消毒、蒸馏等净水过程中,消毒净化程度最高 | |
| C. | 稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢注入水里,并用玻璃棒不断搅拌 | |
| D. | 回收各种白色废弃物品,能有效解决“白色污染”问题 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 兴趣小组的同学用如图所示装置做了相关实验.
兴趣小组的同学用如图所示装置做了相关实验.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 天然气主要成分是乙醇,它是一种有机物 | |
| B. | 充满天然气的管道内部压强要大于大气压 | |
| C. | 天然气是一种高效的能源是因为它的热值比较高 | |
| D. | 天然气中常常要混入一种有特殊气味的气体作为判断气体泄露的警示气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 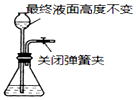 检查装置气密性 | B. | 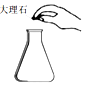 往锥形瓶中加入大理石块 | ||
| C. | 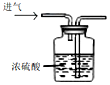 用浓硫酸干燥CO2 | D. |  向下排空气法收集CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com