


 K2MnO4+MnO2+O2↑,
K2MnO4+MnO2+O2↑, K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑; 2H2O+O2↑;因为氧气不易溶于水,并且密度大于空气的密度,除用排水法收集外,还可用向上排空气法收集.故答案为:2H2O2
2H2O+O2↑;因为氧气不易溶于水,并且密度大于空气的密度,除用排水法收集外,还可用向上排空气法收集.故答案为:2H2O2  2H2O+O2↑、向上排空气法.
2H2O+O2↑、向上排空气法.

科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| ① | 取四支试管,各取少量的A、B、C、D溶液,分别滴加紫色石蕊试液 | B溶液变红色,D溶液变成蓝色.A、C溶液都呈 紫 色. |
B是 稀硫酸 D是 澄清石灰水 |
| ② | 另取两支试管,各取少量的A、C溶液,分别先滴入硝酸钡溶液后再滴入稀硝酸溶液. | A中出现白色沉淀,C中无明显现象. |
A是硫酸钠溶液 C是 氯化钠 |
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| ③ | 取该溶液于试管E中,加入硝酸钡溶液后再加入稀硝酸 | 有白色沉淀生成 | 不能确定猜想 2 一定成立 |
| ④ | 取该溶液于试管F中,加入稀盐酸 | 有刺激性气味的气体生成 | 猜想 2、3 可能成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
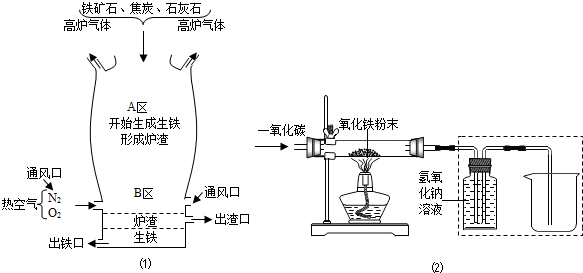
| 物质 性质 |
四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com