
分析 (1)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(2)氯化钠中的阴离子是氯离子,写出其离子符号即可.
(3)化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后.
解答 解:(1)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则2个氮分子可表示为2N2.
(2)氯化钠中的阴离子是氯离子,其离子符号为:Cl-.
(3)由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,故氧化铁中铁的化合价为+3价可表示为:$\stackrel{+3}{Fe}$2O3.
故答案为:(1)2N2;(2)Cl-;(3)$\stackrel{+3}{Fe}$2O3.
点评 本题难度不大,掌握常见化学用语(分子符号、化合价、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:实验探究题
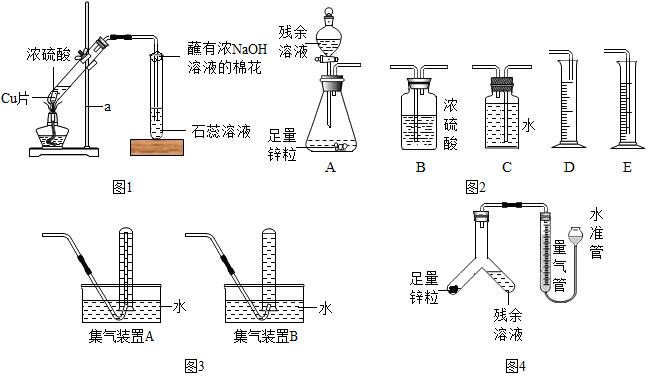
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
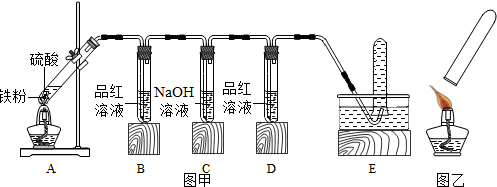
| A中硫酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有二氧化硫和氢气 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
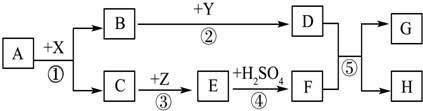
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 如图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
如图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 熟石灰可用来做建筑材料以及中和酸性土壤 | |
| B. | 用水灭火的原理是水降低了可燃物的着火点 | |
| C. | 用C、H2、CO 都可以将CuO 还原成Cu | |
| D. | 燃烧和缓慢氧化都是放热反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 导管口有气泡冒出 | B. | 导管口已无气泡冒出 | ||
| C. | 集气瓶内有大气泡 | D. | 集气瓶口有大气泡冒出 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
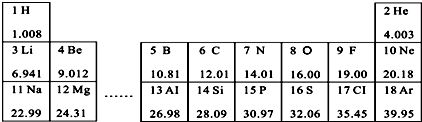
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com