
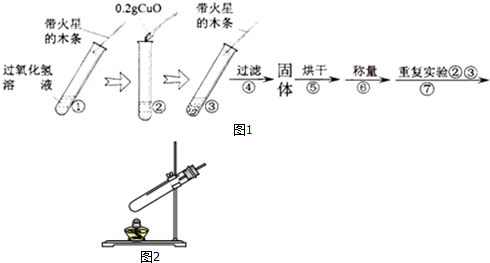
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 剧烈反应,产生大量气泡 带火星的木条复燃 | 0.2g | 溶液中有气泡放出 带火星木条复燃 | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
分析 Ⅲ、根据催化剂的定义回答.
(1)根据氧化铜对过氧化氢的分解有催化作用回答③现象;根据催化剂的定义和特点回答⑥结果;根据催化剂的定义和特点回答⑦现象.
(2)根据对比实验的探究方法回答.
(3)根据过滤的操作过程回答,要注意仪器与材料或用品不同.
(4)根据催化剂化学反应前后的化学性质不变进行解答;
(5)根据过氧化氢分解生成水和氧气进行解答;
(6)根据在加热双氧水的过程中一定会有水蒸气散出,使收集的氧气不纯及收集纯净气体的方法分析.
解答 解:Ⅲ、催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变;故填:质量和化学性质不变;
(1)氧化铜对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象是有气泡,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以氧化铜的质量仍为0.2g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以现象是溶液中有气泡放出,带火星的木条复燃.
(2)为了看氧化铜是否能改变反应的速率,要通过加入氧化铜与不加氧化铜的现象进行对比,才能得出科学合理的结论;
(3)过滤用到的仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒,缺少最后一种,注意仪器与材料或用品不同.
(4)步骤⑦的目的是证明氧化铜的化学性质在反应前后没有发生改变;
(5)过氧化氢分解生成水和氧气,文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气;
(6)在加热双氧水的过程中一定会有水蒸气散出,使收集的氧气不纯,所以将带火星的木条放在导管口没有复燃;为收集到较纯净的氧气,可以采用排水法收集.
故答案为:氧气中混有较多的水蒸气;排水.
故答案为:Ⅲ、质量和化学性质不变;
(1)填表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 剧烈反应,产生大量气泡 | 0.2g | 带火星木条复燃 |
点评 催化剂、催化作用是初中重要基本概念之一,是考查的重点和热点,主要考查对催化剂、催化作用概念的理解,对催化效率影响因素的探究等.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 黄铁矿(主要成分FeS2) | B. | 赤铁矿(主要成分Fe2O3) | ||
| C. | 磁铁矿(主要成分Fe3O4) | D. | 碣铁矿【主要成分Fe2O3•H2O) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
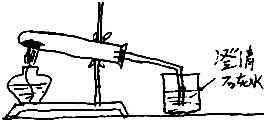 某同学对课本加热铜绿的实验改为如图所示进行,请回答下列问题:
某同学对课本加热铜绿的实验改为如图所示进行,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
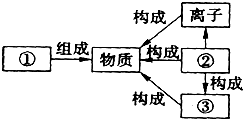
| A. | 表示离子个数的是⑤⑥ | B. | 表示离子所带电荷数的是④⑤ | ||
| C. | 表示分子中原子个数的是③⑦ | D. | 表示分子个数的是①② |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 蜡烛 | 装置Ⅱ | 装置Ⅲ | |
| 反应前的质量/g | 15.8 | 182.3 | 212.2 |
| 反应后的质量/g | 14.4 | 184.1 | 216.6 |

查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | C+O2═CO2 | B. | CaO+H2O═Ca(OH)2 | ||
| C. | CaCO3═CaO+CO2↑ | D. | 2H2O2═2H2O+O2↑ | ||
| E. | HCl+NaOH=NaCl+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂应选用的试剂或操作方法 |
| A | KNO3溶液 | KOH | 加入FeCl3溶液,并过滤 |
| B | Fe2(SO4)3溶液 | CuSO4 | 加入过量铁粉,并过滤 |
| C | HCl | CO2 | 通过NaOH溶液的洗气瓶,再通过浓硫酸的洗气瓶 |
| D | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com