

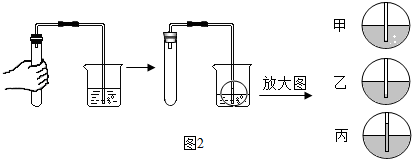
分析 (1)根据实验室中制取二氧化碳的反应原理,根据实验室制取二氧化碳的药品的状态及反应条件确定发生装置,根据收集方法确定收集装置,根据二氧化碳性质分析检验的方法写出反应的化学方程式;
(2)根据检查装置的气密性的方法进行分析解答;
(3)①根据反应物的状态和反应条件来确定制取装置,根据气体的性质来确定收集方法;
②根据高铁酸钾受热分解、与水反应的化学方程式进行分析;
③根据质量守恒定律来分析;根据高铁酸钾与生成氧气的关系式,结合题中的数据进行解答.
解答 解:
(1)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.属于固液常温下反应制取气体,应选用的装置是B,二氧化碳能溶于水密度比空气大,应选用的收集装置是C,二氧化碳能使澄清的石灰水变浑浊,常用澄清的石灰水来检验,反应的方程式是:CO2+Ca(OH)2═CaCO3↓+H2O.故填:BC;CaCO3+2HCl═CaCl2+CO2↑+H2O;Ca(OH)2+CO2═CaCO3↓+H2O;
(2)采用手握试管外壁的方法检查装置的气密性,若装置的气密性良好,导管口会有气泡冒出,将双手移开一会后,烧杯内导管中的液柱会上升;故填:丙;
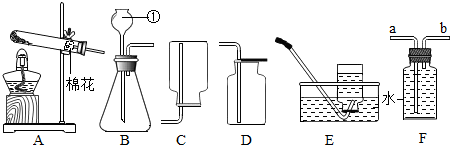
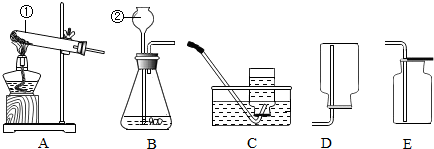
(3)①反应Ⅰ是用固体加热制取氧气,选择装置A来制取;反应Ⅱ是用固体与液体在常温下反应来制取氧气,故选择装置B来制取,因为氧气不易溶于水、密度比空气大,所以可用排水法或向上排空气法来收集,故填:A;B;C(或E);
②通过分析高铁酸钾受热分解、与水反应的化学方程式,都是每792份质量的高铁酸钾生成96份质量的氧气,所以等质量的两份高铁酸钾固体生成的氧气质量相等;故填:相等;
③(i)生成氧气的质量为:10g-9.04g=0.96g;故填:0.96g;
(ii)解:设10g样品中高铁酸钾的质量为x.
4K2FeO4$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+4K2O+3O2↑
792 96
x 0.96 g
$\frac{792}{96}=\frac{x}{0.96g}$
x=7.92 g
所以样品中高铁酸钾的质量分数为:$\frac{7.92g}{10g}×100%$=79.2%
答:此高铁酸钾样品中高铁酸钾的质量分数为79.2%.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.还考查了对化学方程式的认知程度和利用化学方程式进行计算,难度不大,属于基础型考题.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:初中化学 来源: 题型:选择题
| A. | 水中含有氢气和氧气,所以才能被电解 | |
| B. | 电解水时水分子被破坏 | |
| C. | 氢原子和氧原子是电解水变化中的最小微粒 | |
| D. | 水通电分解是化学变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 地球上大部分是含盐量很高的海水 | |
| B. | 淡水资源是取之不尽,用之不竭的 | |
| C. | 为减少水体污染,农药、化肥要合理使用 | |
| D. | 为节约用水,农业、园林浇灌改大水漫灌为滴灌 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
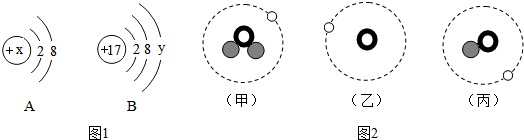
 道耳顿模型特点:不可再分的实心球体
道耳顿模型特点:不可再分的实心球体  汤姆生模型特点:正负电荷均匀分布
汤姆生模型特点:正负电荷均匀分布 卢瑟福模型特点:核位于原子中心,质量集中在核上.
卢瑟福模型特点:核位于原子中心,质量集中在核上. ”表示质子,“
”表示质子,“ ”表示中子,“○”表示电子.请通过比较归纳:
”表示中子,“○”表示电子.请通过比较归纳:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com