
实 验 装 置 | 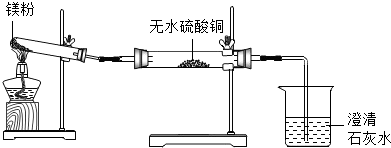 |
| 实 验 现 象 | ①无水硫酸铜粉末逐渐由白色变为蓝色 ②澄清石灰水变浑浊 |
结 论 | 久置的镁粉中除镁元素外,还含有的元素是C、H、O 久置的镁粉中含有碱式碳酸镁 |
分析 氧化镁是白色的粉末;
【查阅资料】根据氧化物的概念分析;
【进行实验】(1)根据实验现象分析;无水CuSO4变成蓝色,说明有水生成,澄清石灰水变浑浊,说明有二氧化碳生成;利用质量守恒定律来分析;
(2)①镁与稀硫酸反应生成硫酸镁和氢气;
②分离难溶性固体与液体可用过滤操作;
【反思与评价】根据镁条所处的环境来分析.
解答 解:氧化镁是白色的粉末,所以镁条表面的“灰黑色外衣”不可能是氧化镁;故填:白色的;
【查阅资料】CO2、SO2和H2O都由两种元素组成,且其中都有氧元素,所以它们都属于氧化物;故填:都属于氧化物;
【进行实验】(1)根据题目可知,无水CuSO4变成蓝色,说明有水生成,澄清石灰水变浑浊,说明有二氧化碳生成,由质量守恒定律可知久置的镁粉中除镁元素外,还含有的元素是C、H、O;故填:C、H、O;
(2)①镁与稀硫酸反应生成硫酸镁和氢气;故填:Mg+H2SO4═MgSO4+H2↑;
②分离难溶性固体与液体可用过滤操作;故填:过滤;
【反思与评价】实验(2)不足以证明镁条表面“灰黑色外衣”中含有碳,因为久置的镁条是放置在常温下的空气环境中,实验(2)是将镁粉在加热且有二氧化碳生成的环境中;故填:久置的镁条是放置在常温下的空气环境中,实验(2)是将镁粉在加热且有二氧化碳生成的环境中.
点评 题通过提出问题、做出猜想、设计实验方案、进行实验等环节,体现了科学探究的一般过程.要求学生对知识掌握程度较高,是一道综合性较强的题目的难题.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
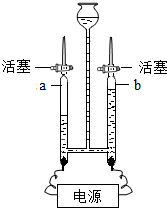 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| V(O2)% | 实验现象 |
| 90% | 燃烧剧烈,燃烧时间长,实验成功 |
| 70% | 燃烧比90%的弱,燃烧时间短,实验成功 |
| 65% | 燃烧比70%的弱,燃烧时间比70%的短,实验成功 |
| 60% | 燃烧比65%的弱,燃烧时间更短,实验成功 |
| 55% | 难以燃烧,只是发红 |
| 实验操作 | 实验现象 |
取3根铁丝,将1根拉直,另两根绕成宽窄不同的螺旋状,进行如图所示实验. | 铁丝均燃烧,剧烈程度不同,II最剧烈,其次是 III,较弱的是 I. |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
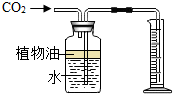 为研究实验室制取二氧化碳的速度与什么因素有关,科学兴趣小组的同学设计了如下实验方案:室温下在六个锥形瓶中分别加入A、B两种产地不同的大理石各50克,然后加入等量的不同溶质质量分数的稀盐酸.记录表如下:
为研究实验室制取二氧化碳的速度与什么因素有关,科学兴趣小组的同学设计了如下实验方案:室温下在六个锥形瓶中分别加入A、B两种产地不同的大理石各50克,然后加入等量的不同溶质质量分数的稀盐酸.记录表如下:| 试验次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 稀盐酸的溶质质量分数 | 5% | 10% | 15% | 5% | 10% | 15% |
| 大理石的种类 | A | A | A | B | B | B |
| 收集一瓶CO2所用的时间/秒 | 45 | 38 | 29 | 56 | 42 | 34 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 印染厂的酸性废水,加入适量的硫酸中和 | |
| B. | 发现有人煤气中毒,立即关闭阀门打开排风扇,将中毒人员转移到空气清新的地方 | |
| C. | 废弃的矿泉水瓶、报纸、金属餐具等物品应回收集中处理 | |
| D. | 被蚊虫叮咬后可以在患处涂抹适量的氢氧化钠溶液减轻痛痒 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com