
����Ŀ��ij��ѧ��ȤС����������װ��̽���������ȡ�����ʡ�������ͼ�ش��й����⣺
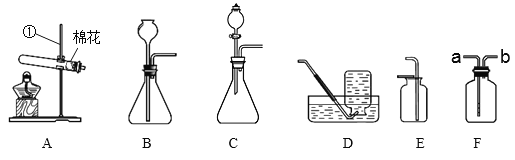
��1��д��װ��ͼ�б�����������ƣ��� __________��
��2��д��ʵ������Aװ����ȡ�����Ļ�ѧ����ʽ____________________��
��3����Eװ�ÿ����ռ�O2��CO2��H2�е�______________������Fװ���ռ�H2������Ӧ��_______����ܿ���ĸ��ͨ�롣
��4��ijͬѧ�ù���������Һ�Ͷ���������ȡO2��Ϊ�˽Ϻõؿ��Ʒ�Ӧ���ʣ���ѡ�õķ���װ����________������ĸ����
��5��Ϊ��̽��������̼�����ʣ�ijͬѧ�������ͼ��ʾ��ʵ�飺
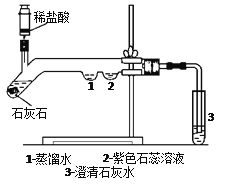
��ʯ��ʯ��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ_________________��
����ע����ע��ϡ���ᣬһ��ʱ��ɹ۲쵽��������________________��____________________��
��6���������������ʵ�飺
��Ũ������������Ի�����_____�ԣ�մ��Ƥ���ϣ����������ô���ˮ��ϴ����Ϳ��3%-5%��̼��������Һ��
��Ũ����Ҳ������ˮ�ԣ���Ũ����ƿ�ǣ�Ũ�������������������______�����������䡱���ߡ���С������
�����⣬Ũ����Ҳ��������ǿ�����ԣ����������������巢����Ӧ���ɵ���ɫ�ķǽ������嵥�ʡ����д̼�����ζ����̬��������������ں�������Һ̬������÷�Ӧ�Ļ�ѧ����ʽΪ________��
�ܽ��Ũ����Ģ٢ڢ����ʿ�֪�������������Ũ����������_________������ĸ���ɶ�ѡ����
A��������̼ B.���� C.���� D.����
���𰸡� ����̨ 2KMnO4 �� K2MnO4��MnO2��O2�� O2��CO2 b C CaCO3��2HCl CaCl2��H2O��CO2�� 2����ɫʯ����Һ���ɫ 3������ʯ��ˮ����� ��ʴ ��С H2SO4��H2S S��SO2��2H2O AD
����������1����ͼ��֪����������̨����2��Aװ�����̹̼����ͣ����Թܿ���һ�����������ü��ȸ�����صķ�����ȡ���������ȸ�����طֽ���ȡ������ͬʱ��������������غͶ������̣��ʷ�Ӧ�Ļ�ѧ����ʽ��2KMnO4 ��K2MnO4 +MnO2 + O2������3��Eװ���������ſ������ռ������װ�ã��������ռ��ܶȱȿ���������塣������̼���������ܶȾ��ȿ����ʸ�װ�ÿ��ռ������������̼���������ܶȱȿ���С�����Ⱦۼ��ڼ���ƿ���ϲ�������Fװ���ռ�����ʱ������Ӧ��b��ͨ�룻��4���������⣬��������Ӵ����������̺�Ӧ��������ʼ��������Ϊ���������ʺ�����������������Ҫ�����䷴Ӧ���ʣ���ͨ�����ƹ�������ļ�������ʵ�֣���Һ©���Ϳ��Կ��Ƽ���Һ��ҩƷ���������ʣ���ѡCװ�ã���5����ʯ��ʯ��ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��CaCO3��2HCl===CaCl2��H2O��CO2��������ע����ע��ϡ���ᣬϡ������̼��Ʒ�Ӧ���ɶ�����̼��������̼��ʹ�����ʯ��ˮ����ǣ�������̼������ˮ��Ӧ����̼�ᣬ̼����ʹ��ɫ��ʯ����Һ��ɺ�ɫ����һ��ʱ����ܹ۲쵽�������ǣ�2����ɫʯ����Һ���ɫ��3������ʯ��ˮ����ǣ���6����Ũ������������Ի�����ǿ�ҵĸ�ʴ�ԣ�մ��Ƥ���ϣ����������ô���ˮ��ϴ����Ϳ��3%-5%��̼��������Һ����Ũ����Ҳ������ˮ�ԣ���Ũ����ƿ�ǣ�Ũ���������տ����е�ˮ�֣������ܼ����������ӣ��������ʵ��������䣬�����������������С���۵���ɫ�ķǽ������嵥�������д̼�����ζ����̬�������Ƕ��������������ں�������Һ̬��������ˮ���ɴ˿�֪�÷�Ӧ�ķ�Ӧ����Ũ��������⣬�����������������ˮ����Ӧ�Ļ�ѧ����ʽ��ʾΪ��H2SO4��H2S==S��SO2��2H2O����Ũ�������백�����������巴Ӧ���ʲ��ܸ������������壬���ܸ��������̼����������ѡAD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʵ���ҳ��õ�ʵ��װ�ã������Ҫ��ش����⣺
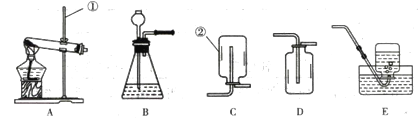
��1��д�����������ƣ��� ____________��______________
��2��ʵ����������غͶ���������ȡO2�Ļ�ѧ����ʽΪ____________________ ��ѡ�õķ���װ����_______����װ����ţ�������Eװ���ռ������壬���˵�ʱ����_________________________________��
��3��ʵ������ȡ���ռ�һ�����Ķ�����̼��Ӧѡ��ķ���װ����_______���ռ�װ����_____���ø÷����ռ�������̼������Ϊ____________________����ʵ������ȡ������̼����Ӧ�Ļ�ѧ����ʽΪ______________________________ ��
��4��ʵ�����ü����������ƺ�����淋Ĺ���������ȡ������������һ����ɫ�д̼�����ζ���ܶȱȿ���С����������ˮ�����壮ʵ������ȡ���ռ�������װ��Ӧѡ��_______����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��Ƽҵ������°����ˡ������Ƽ������ģ���������£�
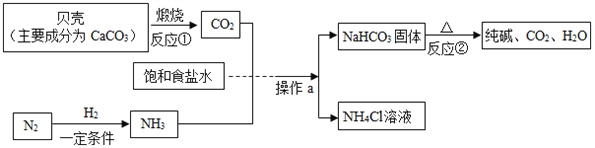
��1����Ӧ�ٵĻ�ѧ����ʽ______________________����Ӧ�ڵĻ�����Ӧ����Ϊ___________��
��2����ҵ�����õ�����������__________��ͬ���ѵ���Һ̬�����з��������
��3������a��������_______��ʵ���ҽ��д˲�������IJ����������ձ�����������_________��
��4�������������п���ѭ�����õ�������____________����д�������õ��ĸ�����NH4Cl��һ����;____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾA��F�dz��л�ѧ���������ʡ�ͼ�С�������ʾת����ϵ����������ʾ��ܷ�Ӧ(�������ʺͷ�Ӧ����δ���)������A���Ϻ�ɫ������B�����������壬C������θҺ�к��е��ᡣ������˵����ȷ���� �� ��

A. Eһ���Ƕ�����̼
B. B����Ϊ������һ����̼
C. �ù�����û���漰�����ֽⷴӦ
D. Dת��ΪA�ķ�Ӧ����Ϊ�û���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ʽ��д��ȷ����
A. S + O2��SO2�� B. Cu+ 2HCl��CuCl2+H2��
C. Fe+CuSO4��FeSO4+Cu D. Ca(OH)2��2HCl��CaCl2��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ֤�����������CO2�������Ը��ڿ�����CO2��������ͼװ�ý���ʵ�顣����˵������ȷ����
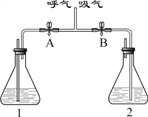
A. ƿ1��ƿ2����װ�Լ���Ϊ����ʯ��ˮ
B. ����ʱ��Ӧ��A��B�رգ�����ʱ�����෴
C. ����ʱ��ƿ1�Լ��г������ݣ�Һ������
D. ͨ��ƿ1��ƿ2�еIJ�ͬ����֤�����������CO2�������Ը��ڿ�����CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ���о���ѧϰ����������������ȷ����
A�����ж����������������Լ���һ��������Ԫ��
B�������ǹ������ʵ�����������ʶ����ɷ��ӹ��ɵ�
C���кͷ�Ӧ���κ�ˮ���ɣ�������κ�ˮ���ɵķ�Ӧһ�����кͷ�Ӧ
D����˿����������ȼ�գ���������������������˿Ҳ���ڿ�����ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ķ�������ն��ġ�
�ճ������У����dz�����Ͱװˮ������ʢ����ǧ��ˮ����ָ��������տ���ˮ���к��д����������Σ�����һ�����ɵ����ж������⣬���������������ڻ����γ�ǿ�°�������-�����������û��°������������
ˮ������������Ҫ��Դ������Ļ�ԭ���ã����˵��¶Ȼ�ʹˮ�е��������࣬�����ͷų��Ļ�ԭø�ɽ�ˮ�е������λ�ԭ���������Ρ�
ͯ���ҡ����Ǿ����˶��������ʵ�飺
ȡ15��Ͱװˮ����ˮ��װ��ã��ֱ��ʹ�ù��̣���̬���в�ͬʱ��ˮͰ�ڵ�ˮ����ȡ13��Ͱװˮ��������ˮ��װ�䣩��̬���ý��м�⡣��������±���
��Ʒ��� | ��̬ʵ����Ʒ��72Сʱ�� | ��̬ʵ����Ʒ��1���£� |
���� | 15 | 13 |
���ﳬ���� | 14 | 2 |
���ﳬ����/% | 93.0 | 15.4 |
���ͣ�ʹ�ù����У���Ͱ��ˮ���ļ��٣���������ˮͰ��Ҳ�������������е��������ʱ��Ͱ��ˮ�»�ﵽ���������ֳ�������¶ȡ�
���ȴ������������κ����Ƿ���Ӱ���أ��ҹ��ڡ�GB 19298-2003ƿ��Ͱ��װ����ˮ���������ж��������Σ���NO2���ƣ��ĺ����涨ΪС��5 ��g/L��
����������ѩ�����˵�ʵ�飺
ȡ���ʵ�Ͱװˮ��������ˮ���ϣ��ⶨ36 h�ڷ������ȣ�����181�Σ���ˮ�����������κ�������NO2���ƣ���������±���
����ʱ��/h | ����/��g/L |
0 | 0.67 |
1 | 0.73 |
3 | 1.12 |
6 | 1.23 |
12 | 1.81 |
24 | 2.44 |
36 | 3.53 |

ȡ����ϸ��14ͰͰװˮ�����飨ÿ��7�ݣ���̬���ã����д�Ż�����⣬�������κ�������NO2���ƣ��������ͼ��
�����ճ���������Ҫ��ȡ�������ε�;�����߲ˣ�ͨ��������Һ��ת������ӽ���������������κ��������300 mg/kg���˲�û����Ϊʳ���߲˶��������������ж����ɴ˿�֪��ǧ��ˮ���е��������β�����ʹ���ж���û����ȷ֤��֤�������������°�������ȷʹ����ˮ����ǰ���£���ǧ��ˮ�������°���������е�ˮ��ֻ�ǻ��Խ����ˣ����ױ�����ϸ�����ա�
�����������ݣ��ش��������⡣
��1��ˮ������������Ҫ��Դ��______��
��2����ʹ�ù����У�Ͱװˮ������������������ֳ��______�йء�
��3������Ϊ��ǧ��ˮ������������˵������______��
��4������ͼ����̬����ʱ��Ӱ��Ͱװˮ���������κ�����������______��
��5�����������º�����ʵ�ʣ�̸̸����Ͱװˮʱ��ע������______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com