

| G | H | |
| 反应前(g) | 57.8 | 40.2 |
| 反应后(g) | 55.4 | 44.6 |
分析 (1)根据反应的原理来分析解答;
(2)根据二氧化碳的性质来分析;
(3)根据实验的注意事项来分析;
(4)根据装置G减少的质量就为氧化铁中氧元素的质量来分析;
(5)根据一氧化碳排出污染空气进行分析.
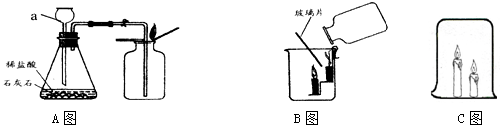
解答 解:(1)大理石与与稀盐酸反应生成氯化钙、水和二氧化碳,在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红,因此实验过程中装置B中的现象是液体由紫色变红色;二氧化碳能使澄清的石灰水变浑浊,故答案为:
液体由紫色变红色;检验二氧化碳是否被除净;
(3)在实验中先通入一氧化碳排净装置内的空气,所以应该先点燃D处的酒精灯;故答案为:D;
(4)G装置内固体减少的质量即为氧化铁中氧元素的质量,即:57.8g-55.4g=2.4g
设氧化铁的质量为x,则x×$\frac{16×3}{56×2+16×3}×100%$=2.4g
x=8g
故答案为:8;
(5)该装置没有尾气处理装置,一氧化碳排出污染空气.故答案为:添加尾气处理装置.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
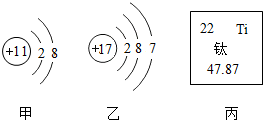
| A. | 甲是钠离子,符号为Na+ | |
| B. | 乙是氯原子,在反应中易得到电子,形成Cl1- | |
| C. | 钛元素是金属元素 | |
| D. | 钛原子内的中子数为26 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 28.6% | B. | 33.3% | C. | 66.7% | D. | 44.8% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com