
| A. | 试管可以直接加热 | |
| B. | 滴瓶上的滴管使用完后应立即清洗 | |
| C. | 温度计可用来搅拌溶液 | |
| D. | 用燃着的酒精灯去引燃另一个酒精灯 |
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:初中化学 来源: 题型:实验探究题

| A中浓硫酸浓度 | 实验现象 | A中生成 气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验Ⅰ | 98% | ① | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验Ⅱ | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ② |
| 实验Ⅲ | 20% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
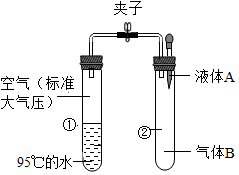 如图所示,夹子开始处于关闭状态,将液体A滴入试管②中与气体B充分反应,打开夹子,可发现试管①中的水立刻沸腾了,则液体A与气体B的组合不可能是( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②中与气体B充分反应,打开夹子,可发现试管①中的水立刻沸腾了,则液体A与气体B的组合不可能是( )| A. | 酒精、氧气 | B. | 水、氨气 | ||
| C. | 硝酸银溶液、氯化氢 | D. | 氢氧化钠溶液、二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
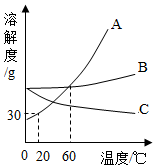 如图为A、B、C三种固体物质的溶解度曲线,回答下列问题:
如图为A、B、C三种固体物质的溶解度曲线,回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
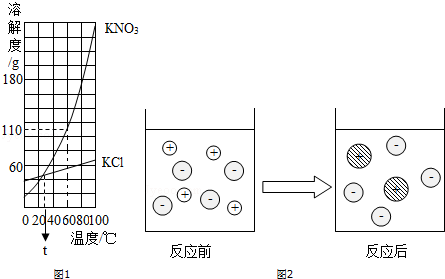
 ”代表的离子Fe3+(填离子符号).
”代表的离子Fe3+(填离子符号). ”的是C(填选项).
”的是C(填选项).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com