
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |


科目:初中化学 来源: 题型:
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | |
| 熔点/℃ | 1535 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
科目:初中化学 来源: 题型:
小亮对铁丝在氧气里燃烧时出现的红热球状物产生了兴趣,随后他进行了以下探究活动。
【问题1】铁燃烧后剩下来的球状物质中还有没有铁呢?
【实验探究】将剩下来的球状物质碾碎,加入 溶液,观察到的现象是 ,说明铁燃烧时溅落下来的黑色物质中还含有铁。
【问题2】铁燃烧的产物为什么不是Fe2O3呢?
【查阅资料】
(1)自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO极易被氧化为Fe2O3);
(2)Fe3O4和Fe2O3的分解温度、铁的熔点见表:
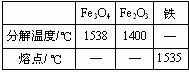
(3)Fe2O3高温时分解成Fe3O4
【理论探讨】实验测定铁在氧气里燃烧的产物是Fe3O4,结合表中数据,可推知铁在氧气里燃烧时产生的高温应在 ℃之间,在此温度范围内 已分解。
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须 ;
(2)有些食品包装盒的透明盖内放有黑色的FeO粉末,若粉末的颜色 ,就说明包装盒破损进气,这样售货员就能及时发现并处理。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com