(2013?滨湖区一模)某品牌纯碱中含有少量氯化钠.某化学探究小组为了测定该纯碱的纯度(即碳酸钠的质量分数),组内一同学设计了如下实验:
【设计实验方案】
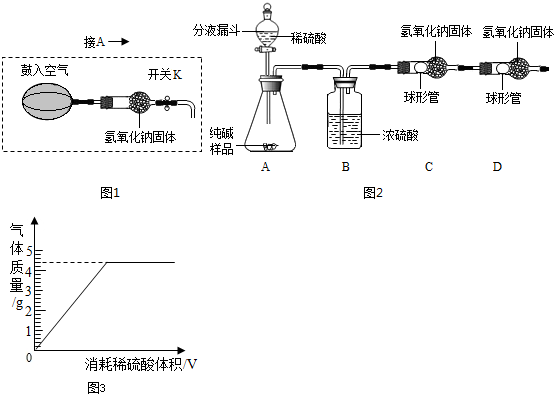
实验装置(如图2所示,固定装置略去,装置内氢氧化钠固体均足量):
需要测定的实验数据:纯碱样品的质量;实验前后C装置的质量.
(1)A装置中反应化学方程式是
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
.为了保证纯碱样品中的碳酸钠完全反应,其操作是逐滴滴入稀硫酸至
不再产生气泡为止
不再产生气泡为止
为止.
(2)B、D装置的作用分别是
除去水蒸气
除去水蒸气
、
防止空气中的二氧化碳和水蒸气进入C装置,影响实验结果
防止空气中的二氧化碳和水蒸气进入C装置,影响实验结果
.
【交流与表达】
(3)图2所示实验装置会造成实验结果偏低,为了克服该不足,有同学提出:将A装置左端与图1装置相连接(须将A装置中双孔橡胶塞换成三孔橡胶塞),反应前、后分别用图1装置缓缓鼓入空气.具体操作是:
①反应前,断开B、C装置之间的连接,用图1装置鼓入一段时间的空气.
②反应后,再次用图1装置鼓入空气,目的是
用不含二氧化碳的空气排出残留在AB装置中反应产生的二氧化碳气体
用不含二氧化碳的空气排出残留在AB装置中反应产生的二氧化碳气体
.
(4)组内另一位同学按照上述装置进行试验,在正确称量C装置的质量时,发现实验前后该装置的质量没有发生变化,可能原因是
装置漏气,产生的二氧化碳气体未被C中的氢氧化钠吸收
装置漏气,产生的二氧化碳气体未被C中的氢氧化钠吸收
.
【数据处理】测定该品牌纯碱的纯度
(5)另取纯碱样品11.0g,加入足量稀硫酸充分反应.产生二氧化碳气体的质量与滴加稀硫酸的体积间数值关系如图3所示.
求:①反应生成CO
2的质量为
4.4
4.4
g.
②通过计算确定食用纯碱粉末中Na
2CO
3的质量分数.(写出计算过程,结果保留一位小数.)
【反思】
(6)若用稀盐酸代替稀硫酸将导致纯碱粉末的纯度
偏高
偏高
(填写“偏高”、“偏低”或“不变”).



 (2012?锦江区二模)(一)如图是已破损的维生素C(简写Vc)说明书部分信息.已知维生素C由碳、氢、氧三种元素组成.请回答:
(2012?锦江区二模)(一)如图是已破损的维生素C(简写Vc)说明书部分信息.已知维生素C由碳、氢、氧三种元素组成.请回答:
