
����Ŀ��ʵ���ϳ������������ķ�ˮ���辭���������ԡ�ij��ȤС��ͬѧ����һ����������������������Һ���������Է�ˮ��
��1�����Լ���ˮ
����ˮ�����Եķ�����_____________��
��2������200 g��������Ϊ5.6%������������Һ
������
m (KOH)=_______g��V(H2O)=________mL��ˮ���ܶȽ���Ϊ1.0 g��mL-1����
����ȡ��������
����������ƽƽ���һֻ�ձ�����������ƽ�����̣�������������Ȼ��______���������Ⱥ�˳������ĸ����ֱ����ƽƽ�⡣
A�����ձ��м���������ͬ�� B������Ҫ�������롢�ƶ�����
����ȡˮ�����ܽ⣻��ת�ơ�
��3�������ⶨ��ˮ
ȡ���Է�ˮ��Ʒ100 g����μ���5.6%������������Һ����ˮ����������������仯������ͼ��ʾ���������ˮ�������ɷֲ����������ط�Ӧ�Ҳ�������أ�
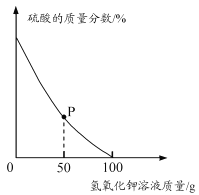
��P���Ӧ��Һ��һ�����ڵ���������_______�������ӷ��ţ���
�����Է�ˮ���������������Ϊ______���ðٷ�����ʾ��������0.1%����
�����㵱��ˮ����������ʱ����Һ������ص�����������д��������̣�����ðٷ�����ʾ��������0.l%����
���𰸡���1��ȡ����������ɫʯ����Һ�������������ԣ������������𰸣�
��2����11.2 188.8 ��BA
��3����K+��H+ ��4.9% ��4.4%
��������
��1��������Һ������Կ������ָʾ������ˮ�к������ᣬ��ô������ɫʯ����Һ�������ǣ�ȡ����������ɫʯ����Һ�������������ԣ�
��2��������200 g��������Ϊ5.6%������������Һ��
��Ҫ�������������ص�����=200g![]() 5.6%=11.2g��
5.6%=11.2g��
��Ҫ���ܼ�ˮ������=200g-11.2g=188.8g ��ˮ�����=![]() =188.8ml ��
=188.8ml ��
��Ҫ��ȡ11.2g���������أ�����������ƽƽ���Ҫ�Ȱ���Ҫ�������롢�ƶ����룬Ȼ�����ձ��м��������ع���ֱ����ƽƽ�⣻
��3�����������غ�ϡ���ᷴӦ��������غ�ˮ����ͼ��֪P��ʱ��Һ�л��������ᣬ��ô��Һ���е����������������أ������е��������������ӣ���ʾΪH+��������е��������Ǽ����ӣ���ʾΪK+��
����ͼ��֪���������غ�ϡ����ǡ����ȫ��Ӧʱ�����ĵ�����������Һ������Ϊ100g�����û�ѧ����ʽ�������������������ᷴӦ�������ȼ��ɼ����ϡ���������ʵ�������
100g����������Һ�����ʵ�����=![]() =5.6g
=5.6g
�����Է�ˮ�����������Ϊx�����ɵ�����ص�����Ϊy��
2KOH + H2SO4 == K2SO4 + 2H2O
112 98 174
5.6g x y
![]() x=4.9g
x=4.9g
���Է�ˮ���������������=![]() 4.9%��
4.9%��
��![]() y=8.7g
y=8.7g
��Ӧ����Һ������=100g+100g=200g
����������ʱ����Һ������ص���������=![]() 4.4%
4.4%
�����Է�ˮ���������������Ϊ4.9%������������ʱ����Һ������ص���������Ϊ4.4% ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ݱ������ҹ���ӡ�����ϳ�Ʊ�����ֳ�Ʊ��������ľ�������ӡ�ƶ��ɣ����и߷�α��Ӳ�Ƚӽ��ڳ�Ʊֽ�����ײ������塢����ʴ��ǿ����ȼ�ա����շ�����ص㣮ij�־������ϣ��仯ѧʽΪ��C9H8O3��n�����ܳ�Ϊ��ӡ�Ʋ��ϣ��ش��������⣺

��1�������������� ��������������
��2��д���������ϵĻ�ѧ���� ��д��һ�����ɣ���
��3����������������C��H��O����Ԫ�ص�����֮��Ϊ ������CԪ�ص����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����Ի�ѧѧϰ�����°빦������������ͼ��ijͬѧ�����������仯����֪ʶ����ͼ��
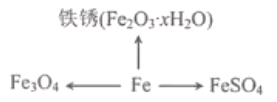
��1������������о���ѧ���ʵ���Ҫ�������� ��˿ȼ������Fe3O4�Ĺ�����________��ѡ�����ų���������������������
�� ����Ʒ����ʴ���̣�ʵ��������������е�______�ȷ�����ѧ��Ӧ�Ĺ��̡�
�� ��FeSO4����Ԫ�ػ��ϼ���ͬ����������Ļ�ѧʽ��______��
��2��������ģ�ͻ����о���ѧ�仯����Ҫ������
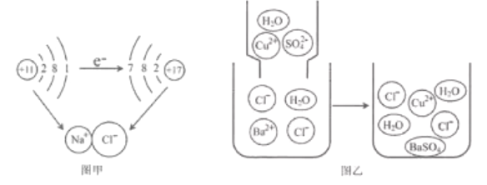
�� ͼ��������������Ӧ���������Ƶ�ʾ��ͼ����ͼ˵���ڻ�ѧ��Ӧ������һ�������仯����________��������ĸ��
a��ԭ�Ӻ� b��ԭ�ӵ����������� c��ԭ�ӵĵ��Ӳ���
�� ͼ��������ͭ��Һ���Ȼ�����Һ��Ӧʾ��ͼ�������ӽǶȷ����û�ѧ��Ӧ�ܷ�����ԭ����_________��
��3�����Ʊ�������ƶԱ�ʵ����ʵ��̽������Ҫ������
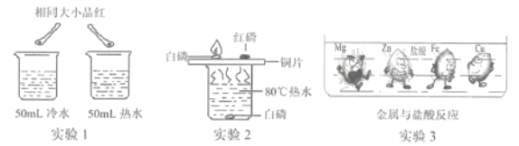
�� ʵ��l ��ͬʱ���ձ��м���һ����ͬ��С��Ʒ�죬��������ˮ����ʱ����ˮ����ˮ�̡�������Ϊ__________��
�� ʵ��2��ʹ��ͭƬ��Ϊ�˶Ա�__________��ͬ��
�� ʵ��3�Ǵ�С��״��ͬ��Mg��Zn��Fe��Cu���ֽ���ͬʱͶ�뵽�����з�������������Χ�ĺڵ��ʾ���ɵ����塣���н��۲���ȷ����__________��������ĸ��
a��ͭ���ܷ����û���Ӧ
b�����ֽ����н��������ǿ����Mg
c����������п�����ֱ������������ᷴӦ��������������Zn��Fe��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йػ�ѧ�����ʾ����ȷ����
A. 2�������ӣ�2Al3+ B. ��ԭ�ӵĽṹʾ��ͼ��![]()
C. �����ӣ�O D. ����þ��þԪ����+2�ۣ�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��HΪ���л�ѧ�������ʣ�����A��EΪ��������EΪ������Һ�壬B��DΪ�H��GΪ���ʣ�CΪʯ��ʯ����Ҫ�ɷ֣�FΪθ�����Ҫ�ɷ֣���Ӧ��Ϊ������ã�����֮������ϵ��ͼ��ʾ�����С�������ʾת����ϵ����������ʾ�֮���ܷ�����Ӧ�����ַ�Ӧ��������Լ���Ӧ����ʡ�ԣ���
��ش��������⣺
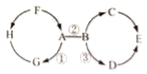
��1��C�Ļ�ѧʽΪ ��E�Ļ�ѧʽΪ ��
��2��B���ʵ�һ����;Ϊ ����Ӧ���Ļ�����Ӧ����Ϊ ��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ���� ���� ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ߴ���������Ʊ���뵼����ϣ��Ʊ��ߴ������Ҫ����������ͼ��ʾ��
��Ϣ��ʯӢɰ����Ҫ�ɷ���SiO2����Ӧ����ѧ����ʽ

��1��ʯӢɰ���� ����������������SiCl4�й�Ԫ�صĻ��ϼ�Ϊ ��д�����������м����CO��һ�ַ��� ��
��2����Ӧ����Ӧ�����ɸߴ����⣬ͬʱ������һ�ֻ������д���˹��̵Ļ�ѧ����ʽ ��
��3����Ӧ�����H2�л���O2���Ӱ�ȫ�Ƕȿ��ǣ���������ĺ���� ��
��4�������ʲ��μӷ�Ӧ�����÷�Ӧ������������������Ϊ9O%�Ĵֹ�2.8�֣�����������Ҫ��̿���ٶ֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ṩ��ʵ��װ�ûش����⡣
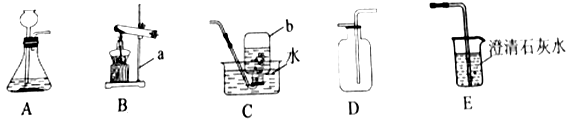
��1��д��ʵ�������ƣ�aΪ_______��bΪ__________��
��2��ʵ������Bװ����ȡO2��������Ӧ�Ļ�ѧ����ʽΪ__________��
��3��ʵ������ȡCO2�ķ������ռ�װ����________������ĸ��ţ���CO2ͨ��Eװ�ÿɹ۲쵽��ʵ��������____________��С����ʵ������Cװ���ռ���һƿCO2��Ϊ��Ū�����е��������ɲ�ȡ�Ŀ�ѧ̬�Ⱥͷ�����_______����������ţ���
����֮���� ���������� ���������� �������ʦ
��4��CO2����NaOH������Ӧ
��ʵ����̡����װ�������ԡ���ͼ��ʾ���Ӻ�װ�á�����ʵ�顣
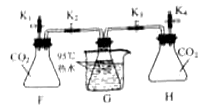
��� | �������� | ʵ������ |
I | ���ɼ�K1���رյ��ɼ�K2��K3��K4����20mLˮע����ƿF�У��رյ��ɼ�K1����ƿF�����ɼ�K2 | ���������� |
II | �رյ��ɼ�K2�����ɼ�K4����20mLNaOH��Һע����ƿH�У��رյ��ɼ�K4����ƿH�����ɼ�K3 | ��ƿG�е���ˮ���ҷ��� |
��ʵ���������ƿG����ˮ���ҷ��ڵ�ԭ����_____________��
��ʵ�鷴˼���й۵���Ϊֻ��Ҫ����ʵ�������������˵��CO2��NaOH������Ӧ����Ըù۵�Ŀ�����________��ѡ������ͬ����������ͬ������������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڵ���̼�����������������
A������̼�ڳ����»�ѧ���ʲ�����
B������̼�ڳ����������ȼ�����ɶ�����̼
C������ʱ����̼��������̼����Ӧ
D������ʱ̼������ͭ��Ӧ����ͭ�Ͷ�����̼
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com