
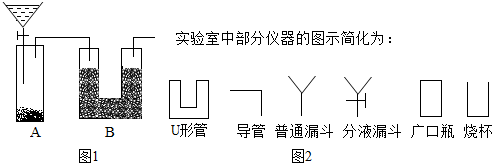
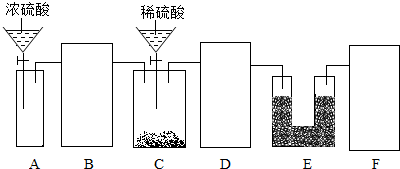
���� ��1�����ݿ����еĶ�����̼��ˮҲ�����ʯ�ҷ�Ӧ����ʯ�һ�����ˮ�ֺͶ�����̼���Լ�װ���ڵ�����Ҳ��ʹʵ����������з�����
��2���ٸ���Ũ��������ˮ�ԣ����Խ����ʯ��֮ǰ����Ҫ����Ũ���Ὣˮ�������գ���Ҫ��ֹ�����е�ˮ�����Ͷ�����̼�����ʯ���н��з�����
�ڸ�������������Ũ������Ҫϡ�ͣ�ʵ������п��ϡ���ᷴӦ�����������������Խ�������̼�ų�����Сʵ�������з�����
�۸���Eװ���������ص�3.52g���Ƕ�����̼��������Ȼ�����û�ѧ����ʽ�����̼���Ƶ������������������������
��3���ٸ���̼���ƺ��Ȼ��Ʒ�Ӧ������̼��Ƴ�����ͨ�����������������̼���Ƶ����������������������
�ڸ���̼���ƺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ�������е����ݽ��м��㣮
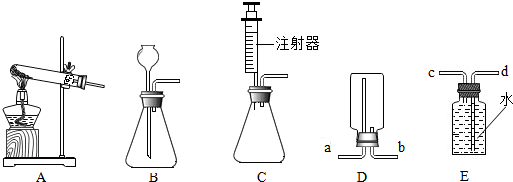
��� �⣺��1�������еĶ�����̼��ˮҲ�����ʯ�ҷ�Ӧ����ʯ�һ�����ˮ�ֺͶ�����̼���Լ�װ���ڵ�����Ҳ��ʹʵ����������Խ�����ݳ����˽ϴ�ƫ����ܵ�ԭ���ǣ���A�в�����CO2����δȫ������B����CO2�л��е�����ˮ��������B����B�����˿����е�ˮ������CO2��
��2����Ũ��������ˮ�ԣ����Խ����ʯ��֮ǰ����Ҫ����Ũ���Ὣˮ�������գ���Ҫ��ֹ�����е�ˮ�����Ͷ�����̼�����ʯ���У�������Ҫ����װ�õ�����ڻ������ʵļ�ͼΪ��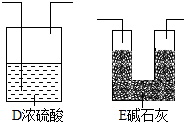 ��
��
������������Ũ������Ҫϡ�ͣ�ʵ������п��ϡ���ᷴӦ�����������������Խ�������̼�ų�����Сʵ��������Aװ�õĹ��ƿ��Ӧ������Լ��ǣ�ZnƬ������ˮ����װ�õ������ǣ�����A�����ɵ�H2��C�е�CO2ȫ������E�б���ʯ�����գ�
����μӷ�Ӧ��̼���Ƶ�����Ϊx��
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
x 3.52g
$\frac{106}{x}$=$\frac{44}{3.52g}$
x=8.48g
���Ը�Na2CO3�����Ĵ���Ϊ��$\frac{8.48g}{10g}$��100%=84.8%��
��3����̼���ƺ��Ȼ��Ʒ�Ӧ������̼��Ƴ�����ͨ�����������������̼���Ƶ�������������������������Բ��������ǣ� ��
��
��ʵ��ʱ������Ʒ������Ϊa�ˣ��������ʵ�����Ϊb�ˣ�����̼�������Ϊb����μӷ�Ӧ��̼��������Ϊy������
CaCl2+Na2CO3=CaCO3��+2NaCl
106 100
y bg
$\frac{106}{y}$=$\frac{100}{bg}$
y=$\frac{53b}{50}$g
����̼��Ƶ���������Ϊ��$\frac{\frac{53b}{50}g}{ag}$��100%=$\frac{53b}{50a}$��
�ʴ�Ϊ����1����A�в�����CO2����δȫ������B����CO2�л��е�����ˮ��������B����B�����˿����е�ˮ������CO2��
��2����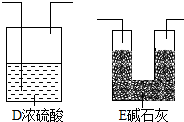
��ZnƬ������ˮ������A�����ɵ�H2��C�е�CO2ȫ������E�б���ʯ�����գ�
��84.8%��
��3����
��$\frac{53b}{50a}$��
���� �ڽ������ʱ�����ȷ������п�������⣬Ȼ����ѧ����֪ʶ��������������ʾ���н��


 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
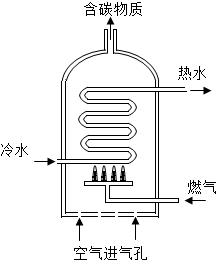 ͨ����ѧѧϰ��ͬѧ�Ƕ����ʵ���ɡ��ṹ�����ʼ���;����һ�����˽⣮
ͨ����ѧѧϰ��ͬѧ�Ƕ����ʵ���ɡ��ṹ�����ʼ���;����һ�����˽⣮| ȼ�� | ���ȼ�ղ��������/g | |
| CO2 | SO2 | |
| ���� | 2900 | 5.0 |
| ��Ȼ�� | 2500 | 0.1 |
| ú | 2500 | 11.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3 NaCl KNO3 | B�� | NaCl NaOH NaNO3 | ||
| C�� | CaCl2 NaNO3 Na2CO3 | D�� | KNO3 H2SO4 NaCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ��� | ʵ����ʵ | ʵ����� |
| A | ��ȼ�ŵ�ľ������ʢ��ij��ɫ����ļ���ƿ�У�����Ϩ�� | ������һ���Ƕ�����̼ |
| B | ��ij��ɫ��Һ������ɫ��̪��Һ���ʺ�ɫ | ����Һһ���Ǽ���Һ |
| C | ��ij�����м���ϡ���ᣬ�������� | ������һ����̼���� |
| D | �����£����ij��Һ��pH=0 | ����Һһ�������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
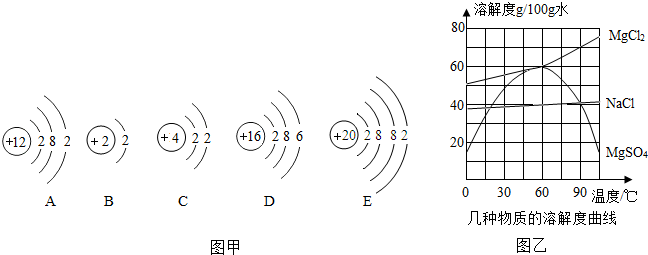
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ���� | ���� | ˮ | ������̼ | X |
| ��Ӧǰ����/g | 6.0 | 12.8 | 0 | 0 | 0 |
| ��Ӧ������/g | 0 | 0 | 7.2 | 8.8 | a |
| A�� | X����̼���⡢��Ԫ�� | B�� | X�����Ǹ÷�Ӧ�Ĵ��� | ||
| C�� | ����a��ֵ��ȷ�� | D�� | X��һ����̼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 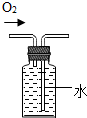 �ռ�O2 | B�� | 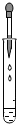 �μ�Һ�� | ||
| C�� |  ����ҺpH | D�� | 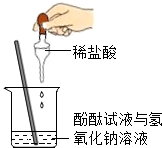 ����к� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com