



 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
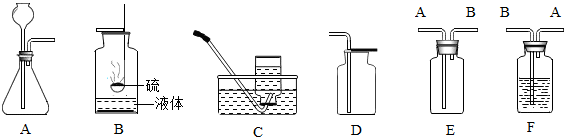 A来制取氧气,写出该反应的化学方程式
A来制取氧气,写出该反应的化学方程式
| ||
| ||
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样,分别用玻璃棒蘸取四种溶液,滴到pH试纸上,与标准比色卡对照 | B的溶液的pH<7,其余溶液的pH>7 | B是 稀硫酸(或H2SO4) 稀硫酸(或H2SO4) 溶液 |
| ②取三支试管,各取少量的A、C、D溶液,分别滴加稀盐酸 | A是碳酸钠溶液 | |
| ③取两支试管,各取少量的C、D溶液,用玻璃管分别吹入CO2 | C是饱和石灰水 |
| 两两混合 | A+B | B+C | C+D | A+D |
| 实验现象 | ↓ | ↑ | / | / |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A | B | C | D | |
| A | - | ↓ | ↑ | |
| B | - | ↓ | ↓ | |
| C | ↓ | ↓ | ↓ | |
| D | ↑ | ↓ | ↓ |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样,分别用玻璃棒蘸取四种溶液,滴到pH试纸上,将试纸显示的颜色与标准比色卡对照 | B溶液的pH<7,其它溶液的 pH>7 |
B是 稀硫酸 稀硫酸 |
| ②取三支试管,各取少量的A、C、D溶液,分别滴加稀盐酸 | D无明显现象A中有气泡冒出 D无明显现象A中有气泡冒出 |
A是碳酸钠溶液 |
| ③另取两支试管,各取少量的C、D溶液,用玻璃管分别通入二氧化碳气体 | D无明显现象,C中出现白色沉淀 D无明显现象,C中出现白色沉淀 |
C是饱和石灰水 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 实验现象及结论 |
1.取少量B、C的粉末分别放入两支洁净的试管中,分别加入足量水,充分振荡后,观察; 2.向两支试管中分别滴加氯化钡溶液. 1.取少量B、C的粉末分别放入两支洁净的试管中,分别加入足量水,充分振荡后,观察; 2.向两支试管中分别滴加氯化钡溶液. |
两支试管中均为无色澄清溶液; 出现白色沉淀的原物质是K2SO4;仍是澄清溶液的原物质是KCl. 两支试管中均为无色澄清溶液; 出现白色沉淀的原物质是K2SO4;仍是澄清溶液的原物质是KCl. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com