
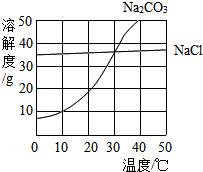
 图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.
图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.分析 从图中可以看出氯化钠的溶解度受温度变化影响不大,所以在改变温度时,氯化钠在水中的溶解能力基本保持不变.而碳酸钠的溶解度受温度变化影响较大,所以在改变温度时,碳酸钠在水中的溶解能力会发生较大的改变.
解答 解:从溶解度曲线图中可以看出在温度等于30℃时,氯化钠的溶解度与碳酸钠的溶解度相同.同时也能看出碳酸钠的溶解度受温度影响较大,当温度升高时,溶解度升高,所以在夏天,虽然水分蒸发但碳酸钠的溶解能力变大,碳酸钠不析出.冬天时温度降低碳酸钠析出.而氯化钠的溶解度受温度影响较小,所以在夏天时,虽然温度升高了,但水分少了,所以氯化钠析出.而冬天时,温度虽然降低,但氯化钠的溶解能力变化不大,所以没有析出.
故答案为:(1)当温度为30℃时,氯化钠的溶解度与碳酸钠的溶解度相同.
(2)氯化钠的溶解度受温度影响不大,夏天温度高水分蒸发快,氯化钠易结晶析出;碳酸钠的溶解度受温度影响大,夏天温度高,溶解能力变大,冬天温度低,碳酸钠易结晶析出,而氯化钠的溶解能力变化小不析出;所以“夏天晒盐”“冬天捞碱”.
点评 氯化钠的溶解度受温度影响较小,所以在夏天时温度虽然升高,溶解能力变化小,但水分挥发所以氯化钠析出.


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:初中化学 来源: 题型:选择题
| A. | 粗盐研细是为了增大食盐的溶解度 | |
| B. | 过滤时液体的液面要低于滤纸边缘 | |
| C. | 加热蒸发时不断搅拌直至水分全部蒸干 | |
| D. | 实验结束随即将蒸发皿取下放在桌面上 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 5.85g | B. | 11.7g | C. | 17.55g | D. | 160.3g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g/100g水) | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 复分解反应 | B. | 化合反应 | C. | 置换反应 | D. | 分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com