
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 质量 | B. | 原子总数 | C. | 碳原子数 | D. | 密度 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
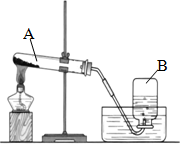 通过化学学习,应该知道有多种途径可以制取氧气.如:
通过化学学习,应该知道有多种途径可以制取氧气.如:

| 实验 序号 | 过氧化氢 溶液浓度/% | 过氧化氢 溶液体积/mL | 温度/℃ | 二氧化锰 的用量/g | 收集氧气 的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| ③ | 30 | 5 | 35 | / | 2 | 49.21 |
| ④ | 30 | 5 | 55 | / | 2 | 10.76 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com