
【题目】(6分)为了减少空气中的温室气体,并且充分利用二氧化碳资源,科学家们设想了一系列捕捉和封存二氧化碳的方法。
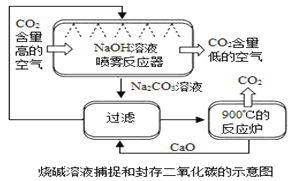
烧碱溶液捕捉和封存二氧化碳法(见上图):
①喷雾反应器中,发生反应的化学方程式为 ,NaOH溶液喷成雾状的目的是 。
②过滤环节中所得滤渣的主要成分是 ,请用化学方程式说明原因: , 。
③在整个流程中,循环利用的物质有 。
【答案】①2NaOH+CO2=Na2CO3+H2O 增大反应物间接触面积,使反应更充分
②CaCO3 CaO+H2O=Ca(OH)2 Na2CO3+ Ca(OH)2= CaCO3↓+2NaOH
③CaO、NaOH
【解析】
试题分析:①喷雾反应器中是将含二氧化碳高的空气通入到NaOH溶液中去,发生反应的化学方程式为:2NaOH+CO2=Na2CO3+H2O ;NaOH溶液喷成雾状的目的是:增大反应物间接触面积,使反应更充分
②将CaO和Na2CO3溶液放在一起,发生反应:CaO + H2O === Ca(OH)2,Na2CO3+ Ca(OH)2= CaCO3↓+2NaOH ,故过滤环节中所得滤渣的主要成分是CaCO3
③从流程图中看出,过滤后得到的滤液(NaOH溶液)又加入到了喷雾反应器中,而在900℃的反应炉中生成的CaO也加入到了Na2CO3溶液中,故在整个流程中,循环利用的物质有CaO、NaOH


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】甲、乙两种不含结晶水的固体物质的溶解度曲线如下图,下列说法中正确的是

A.甲的溶解度比乙大
B.t1℃时,甲的饱和溶液中溶质与溶液的质量比为1∶5
C.t2℃时,甲、乙的两种溶液中溶质的质量分数相等
D.将等质量甲、乙的两种饱和溶液分别由t3℃降温至t2℃,析出甲的质量一定比析出乙的质量大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室用大理石与稀盐酸反应制取CO2,反应后所得溶液体积为40mL.(假设大理石中的杂质不与盐酸反应,反应前后溶液体积不变).向该溶液中匀速逐滴加人Na2CO3溶液 并不断搅拌,测得溶液的pH随时间变化如图所示,该过程 共放出气体660mL(密度为2.0g/L)析出沉淀5.0g.
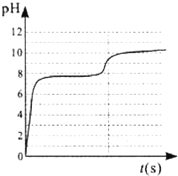
(1)根据图象可以看出.Na2CO3首先与溶液中的 反应.
(2)本实验制取CO2所用大理石中含CaCO3 g.
(3)已知制取CO2所用稀盐酸的密度为1.06g/Cm3求这种盐酸的质量分数.(计算结果保留1位小数,无计算过程不给分)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(3分)汽车尾气排放出的气体主要有NO和NO2,它们污染环境,可用氨气(NH3)除去。反应的化学方程式为:2NH3+NO+NO2催化剂2N2+3H2O。若反应后得到56gN2,理论上消耗氨气多少克?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com