
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
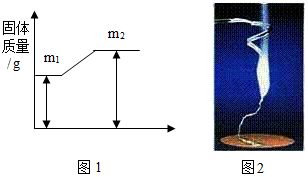
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 在天平左右两盘中各放一个等质量的烧杯,烧杯中分别盛有等质量的足量的稀硫酸,天平平衡.向左盘烧杯中加入27g氧化钙,向右盘烧杯中加入铁粉,若天平最终平衡,则加入铁粉的质量为( )
在天平左右两盘中各放一个等质量的烧杯,烧杯中分别盛有等质量的足量的稀硫酸,天平平衡.向左盘烧杯中加入27g氧化钙,向右盘烧杯中加入铁粉,若天平最终平衡,则加入铁粉的质量为( )| A. | 24g | B. | 26g | C. | 27g | D. | 28g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
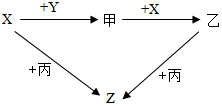 X、Y、Z、甲、乙、丙均为初中化学中常见的物质,其中X、Y、Z为单质,Z为红色固体,甲、乙、丙为氧化物.它们之间在一定条件下存在如图所示的转化关系.
X、Y、Z、甲、乙、丙均为初中化学中常见的物质,其中X、Y、Z为单质,Z为红色固体,甲、乙、丙为氧化物.它们之间在一定条件下存在如图所示的转化关系.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com