
【题目】分析处理图表中的信息是学习化学的一种重要方法。
(1)下表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 |
①40℃时,氯化钠的溶解度为_____g。
②碳酸钠的溶解度随温度的升高而________(填“增大”或“减小”)。在20℃时,将100g的水加入30 g碳酸钠中,充分搅拌后得到的是________(填“饱和溶液”或“不饱和溶液”)。
③10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是______。
(2)将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式_______。右图是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是_______(填标号)。

【答案】(1)① 36.6 ② 增大 饱和溶液 ③碳酸钠饱和溶液
(2)Fe+2HCl=FeCl2+H2↑ AC
【解析】
试题分析:(1)由表格可知,①40℃时,氯化钠的溶解度为36.6g;故填:36.6;②碳酸钠的溶解度随温度的升高而增大;在20℃时,碳酸钠的溶解度为21.8g,也就是在该温度下的100g水中最多溶解碳酸钠21.8g,此时加入30g不能完全溶解,形成了该温度下的饱和溶液,③10℃时,分别配制表中两种物质的饱和溶液,该温度下,溶解度小的,饱和溶液中溶质的质量分数越小,故填:碳酸钠饱和溶液;(2)根据金属的活动性顺序可知,铁与稀盐酸反应生成氯化亚铁和氢气,而铜与稀盐酸不反应;随着反应的进行,氢气的质量增加,当铁完全反应后,氢气的质量不再改变;随着铁的反应,金属混合物的质量不断减小,当铁完全反应后,剩余固体是铜.故填:Fe+2HCl=FeCl2+H2↑;AC.


科目:初中化学 来源: 题型:
【题目】下列物质中,前者属于纯净物,后者属于混合物的是( )
A.净化后的空气、氧化镁 B.氧化铜、液氧
C.生锈的铁钉、五氧化二磷 D.水和冰相混合、啤酒
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有两种外观类似黄金的制品①Cu-Ag合金和②Cu-Zn合金,若实验室只提供一瓶稀硫酸和必要仪器。
(1)你认为能测出合金 (填序号)中铜的质量分数。
(2)取上述(1)中合金粉末20g放入烧杯中,加入50g的稀硫酸,恰好完全反应, 烧
杯内剩余物质的质量为69.8g。求:
①根据质量守恒定律,产生氢气的质量为 g。
②求所用稀硫酸的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~F是初中化学常见的物质,已知C物质是一种常用的建筑材料,常用来砌砖和粉刷壁。六种物质之间的关系如右图所示,图中 “![]() ”表示物质间的转化关系,“—”表示两端物质能相互反应(部分反应物、生成物及反应条件未标出),E和F反应生成白色沉淀且沉淀不溶于稀硝酸。
”表示物质间的转化关系,“—”表示两端物质能相互反应(部分反应物、生成物及反应条件未标出),E和F反应生成白色沉淀且沉淀不溶于稀硝酸。
请回答下列问题:
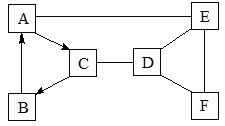
(1)写出下列物质的化学式:A ;E ;F 。
(2)写出物质C和D反应的化学方程式: 。该反应属于化学反应基本类型中的 反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知某Na2SO4样品中混有少量的碳酸钠,某化学实验小组取样品20克,加入50克水后搅拌,样品全部溶解。向其中逐滴加入溶质质量分数为10%的稀硫酸,直到不再产生气泡为止,共用去10%的稀硫酸9.8克,请计算:(计算结果保留一位小数)
(1)样品中Na2SO4的质量分数。
(2)反应后所得溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在某种细菌作用下,氨气(NH3)和氧气可处理含甲醇(CH3OH)的工业废水。
计算下列问题:
(1)NH3的相对分子质量为 ;
(2)CH3OH中氧气元素的质量分数(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a、b两种物质的溶解度曲线如右图所示。下列说法不正确的是

A.将![]() ℃时b的饱和溶液加水可变为不饱和溶液
℃时b的饱和溶液加水可变为不饱和溶液
B.将![]() ℃时a的饱和溶液降温至
℃时a的饱和溶液降温至![]() ℃,溶液质量不变
℃,溶液质量不变
C.![]() ℃时,两种物质的饱和溶液中溶质质量分数a
℃时,两种物质的饱和溶液中溶质质量分数a![]() b
b
D.将![]() ℃时a、b的饱和溶液分别降温至
℃时a、b的饱和溶液分别降温至![]() ℃,两溶液的溶质质量分数相等
℃,两溶液的溶质质量分数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com