
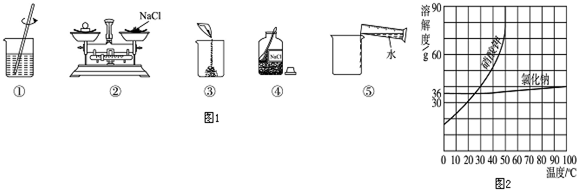
分析 (1)粗盐提纯是将粗盐中含有的泥沙等不溶物除去,结合蒸发操作中玻璃棒的作用,据此进行分析解答;
(2)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答;
(3)根据基本实验操作要求来分析;
(4)溶质质量=溶液质量×溶质质量分数,溶剂质量=溶液质量-溶质质量;
(5)根据溶质质量分数的计算方法考虑;
(6)根据溶解度考虑加入的溶质是否全部溶解再进行计算.
解答 解:(1)在粗盐提纯时,首先要将粗盐配成溶液,然后用过滤的方法将泥沙除去,再对滤液进行蒸发操作使晶体逐渐的析出,在蒸发操作中,玻璃棒起到搅拌而使液体受热均匀的作用,防止局部温度过高,造成液滴飞溅,还能起到转移固体的作用.
故答案为:①溶解;②过滤;③蒸发;④结晶;搅拌,防止局部温度过高,造成液滴飞溅;
(2)配制溶质质量分数为100g10%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,故纠正错误后,配制溶液的正确操作顺序为④②③⑤①.故填:④②③⑤①;
(3)图②操作,将药品与砝码的位置放反了,故填:②;
(4)氯化钠质量:100g×10%=10g,需水:100g-10g=90g,水体积:$\frac{90g}{1g/ml}$=90mL;故填:10;90;
(5)不慎将少量食盐洒落在桌面上,溶质少了,导致溶质质量分数小了;故填:<;
(6)20℃时,NaCl溶解度为36g说明100g水中最多溶36g,所以溶液质量为36g+100g=136g,溶质质量分数为:$\frac{36g}{136g}$×100%=26.5%;故填:136;26.5%.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、注意事项等是正确解答本题的关键.


 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图所示.将蜡烛与绿色植物一起放在黑暗密闭的玻璃罩内,一个月后观察到的现象是( )
如图所示.将蜡烛与绿色植物一起放在黑暗密闭的玻璃罩内,一个月后观察到的现象是( )| A. | 植物活着、蜡烛熄灭 | B. | 植物死亡、蜡烛燃尽 | ||
| C. | 植物活着、蜡烛燃尽 | D. | 植物死亡、蜡烛熄灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
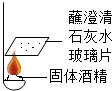 在一次用餐时,小华对燃料“固体酒精”产生了好奇,于是对其成分进行探究:
在一次用餐时,小华对燃料“固体酒精”产生了好奇,于是对其成分进行探究:| 方案 | 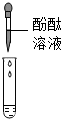 | 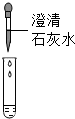 |
| 现象 | 溶液变红 | 产生 白色沉淀 |
| 结论 | 溶液中有氢氧化钠 | 溶液中由碳酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 反应前后原子的种类发生改变 | |
| B. | 图示中共有4种分子 | |
| C. | 该图示说明在化学变化中分子可分,原子不可分 | |
| D. | 以上反应符合质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Ca(HCO3)2$\stackrel{加热}{→}$CaCO3+CO2+H2O | B. | Mg+H2SO4→MgSO4+H2 | ||
| C. | Fe+O2$\stackrel{点燃}{→}$Fe3O4 | D. | C2H5OH+O2$\stackrel{点燃}{→}$CO2+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com