
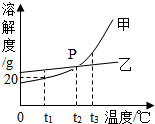
 甲、乙两种不含结晶水的固体物质的溶解度曲线如图:
甲、乙两种不含结晶水的固体物质的溶解度曲线如图:分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,图中交点P表示的一条意义是:在t2℃时,甲乙两物质的溶解度相等;
(2)t1℃时,甲物质的溶解度是10g,所以50g甲的饱和溶液中所含溶质小于10g;
(3)t2℃时的甲、乙两种物质的饱和溶液的溶解度相等,溶质质量分数相等,所以升温至t3℃(溶剂的量不变),不会析出晶体,甲溶液中溶质的质量分数等于乙溶液中的溶质的质量分数;
(4)甲物质的溶解度受温度影响变化较大,所以甲物质的饱和溶液中含有少量乙,可采用降温结晶的方法分离提纯甲,原理是:甲的溶解度随温度的升高显著增大,乙的溶解度受温度的影响不大,所以温度降低,甲大量结晶析出,乙留在剩余溶液中.
故答案为:(1)在t2℃时,甲乙两物质的溶解度相等;
(2)小于;
(3)等于;
(4)降温;甲的溶解度随温度的升高显著增大,乙的溶解度受温度的影响不大,所以温度降低,甲大量结晶析出,乙留在剩余溶液中.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


科目:初中化学 来源: 题型:实验探究题
| 实验操作与现象 | 实验结论 |
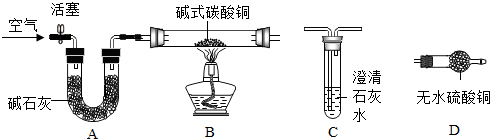
| 取黑色粉末,加入足量稀硫酸,充分反应后,黑色固体全部溶解形成蓝色溶液 | 猜想②正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.认识物质俗名 | B.注意实验安全 |
| ①冰一固体二氧化碳 ②熟石灰--氧化钙 | ①鉴别化学药品时可以品尝 ②可以直接去闻浓盐酸的气味 |
| C.合理利用资源 | D.健康生活方式 |
| ①合理使用农药、化肥提高农业产量 ②用人畜粪便、作物秸秆制取沼气 | ①药补不如食补,要均衡膳食 ②少量吸烟,可以使精神提高 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaHCO3是纯碱 | |
| B. | 析出晶体后剩余溶液中溶质只有NH4Cl | |
| C. | 配制饱和食盐水时,可通过搅拌来提高食盐的溶解度 | |
| D. | 向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
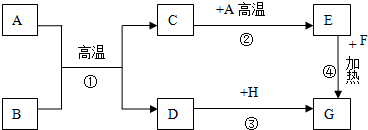
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com