
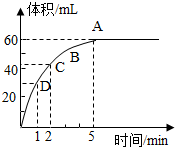
 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2 粉末于50mL密度为1.1g?cm-3 的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示.请依图回答下列问题:
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2 粉末于50mL密度为1.1g?cm-3 的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如图所示.请依图回答下列问题:分析 反应方程式为:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应为不可逆反应,在5min后,收集到的气体体积不再增加,说明过氧化氢完全分解,根据图象可知生成的氧气的体积,随着反应的进行,溶液的浓度逐渐降低,反应速率逐渐减小.
解答 解:(1)由反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应为不可逆反应,在5min后,收集到的气体体积不再增加,说明过氧化氢完全分解,由图象可知,生成氧气的体积为60mL,故答案为:60ml;
(2)由图象可知,当时间进行到1min时,需要的时间为1min,故答案为:1 min;
(3)反应物浓度大小决定反应速率大小,随着反应的进行,双氧水的浓度逐渐减小,反应速率也随着减小,
故答案为:D>C>B>A;
(4)浓度越大,反应速率越大,反之越小,随着反应进行,反应物的浓度逐渐减小,则速率逐渐减小,
故答案为:随着反应的进行,双氧水的浓度逐渐减小,反应速率也随着减小;
(5)该反应为不可逆反应,在5min后,收集到的气体体积不再增加,说明过氧化氢完全分解,
故答案为:此时双氧水已完全分解.
点评 本题考查过氧化氢分解的速率曲线,题目难度不大,主要考查浓度对反应速率的影响,注意对图象的分析.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 结论 |
| 将一定量的NaCl溶于水,滴入2滴酚酞 | 溶液不显红色 | 猜想一不成立 |
| 向一定量的蒸馏水中滴入2滴酚酞 | 溶液不显红色 | 猜想二不成立 |
| 将一定量的Na2CO3溶于水,滴入2滴酚酞,再向溶液中加入适量的CaCl2 | 溶液先显红色,加入CaCl2后红色消失,出现白色沉淀 | 猜想三成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

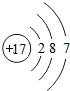 ,该元素的原子在化学反应中比较容易得到(填“得到”或“失去”)电子变成阴(填“阴”或“阳”)离子,形成的离子符号为Cl-.
,该元素的原子在化学反应中比较容易得到(填“得到”或“失去”)电子变成阴(填“阴”或“阳”)离子,形成的离子符号为Cl-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com