
分析 碳酸钙在高温下分解生成氧化钙和二氧化碳;由质量守恒定律,固体物质减少的质量即为生成二氧化碳气体的质量,由反应的化学方程式计算出参加反应的碳酸钙的质量即可;由剩余固体的质量为10g,剩余固体中钙元素的质量分数为48%,计算出钙元素的质量,进而由反应前后钙元素的质量不变,计算出石灰石样品中碳酸钙的质量及质量分数即可.
解答 解:(1)由质量守恒定律,生成二氧化碳气体的质量为14.4g-10g=4.4g.
设参加反应的碳酸钙的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 4.4g
$\frac{100}{44}=\frac{x}{4.4g}$ x=10g
(2)剩余固体的质量为10g,剩余固体中钙元素的质量分数为48%,则钙元素的质量为10g×48%=4.8g;反应前后钙元素的质量不变,则石灰石样品中碳酸钙的质量为4.8g÷($\frac{40}{100}$×100%)=12g.
石灰石样品中碳酸钙的质量分数为$\frac{12}{14.4}$×100%≈83.3%.
答:(1)参加反应的碳酸钙的质量为10g;(2)石灰石样品中碳酸钙的质量分数为83.3%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳气体的质量是正确解答本题的前提和关键.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 铁丝中含碳量 | 0.05% | 0.2% | 0.6% |
| 燃烧时的现象 | 剧烈燃烧,极少火星 | 剧烈燃烧,少量火星 | 剧烈燃烧,大量火星 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
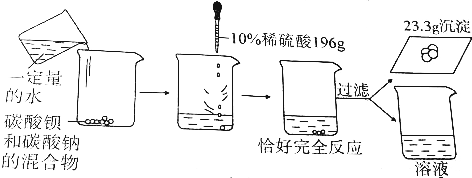
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
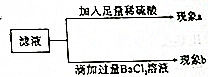 在做课本纯碱的化学性质分组实验时,第-组学生进行Na2CO3与BaC12溶液的反应,第二组学生进行Na2CO3与H2SO4溶液的反应.
在做课本纯碱的化学性质分组实验时,第-组学生进行Na2CO3与BaC12溶液的反应,第二组学生进行Na2CO3与H2SO4溶液的反应.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用硫酸铜溶液鉴别氢氧化钠和碳酸钠溶液 | |
| B. | 用紫色石蕊试液测定雨水的酸碱度 | |
| C. | 往固体中加入稀盐酸,出现气泡说明该固体一定是碳酸盐 | |
| D. | 只用酚酞试液就能将氯化钠溶液、氢氧化钠溶液、盐酸区别开来 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食品包装袋中充入氮气以防腐 | B. | 氧气可用作火箭发射的燃料 | ||
| C. | 稀有气体可制成闪光灯 | D. | 二氧化碳可作温室中的气体肥料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com