

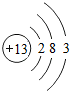 ,该原子在化学反应中易失(填“得”或“失”)电子,形成的离子符号为Al3+铜和稀硫酸不反应,与浓硫酸在一定条件下可以反应,其化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+X↑+2H2O,则X的化学式为SO2.
,该原子在化学反应中易失(填“得”或“失”)电子,形成的离子符号为Al3+铜和稀硫酸不反应,与浓硫酸在一定条件下可以反应,其化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+X↑+2H2O,则X的化学式为SO2. 分析 (1)a、根据区分硬水和软水的方法分析回答;
b、根据氯化镁、氯化钙的性质分析回答;
(2)根据金属的性质和用途分析回答;
(3)根据原子结构示意图的意义、质量守恒定律反应前后原子的种类没有改变,数目没有增减进行解答.
解答 解:(1)a、区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水;
b、如果某地下水钙、镁离子含量过高(假设主要以 CaCl2、MgCl2形式存在),可先加入适量的熟石灰,反应的化学方程式为:MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2,再加入适量的碳酸钠后生成沉淀碳酸钙,即可将水软化;
(3)由铝的原子结构示意图可知,最外层电子数是3,小于4,该原子在化学反应中易失电子,形成铝离子,符号为Al3+;在反应的化学方程式Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+X↑+2H2O中,反应物中铜、氢、硫、氧原子个数分别为1、4、2、8,反应后的生成物中铜、氢、硫、氧原子个数分别为1、4、1、6,根据反应前后原子种类、数目不变,则X中含有1个硫原子和2个氧原子,则物质X的化学式为SO2.
故答案为:(1)a、用肥皂水;b、MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2,碳酸钠;(3)失,Al3+;SO2.
点评 本考点属于结合课本知识的信息,也体现了性质决定用途,用途反映性质的理念.还结合了新课标中的一个新的考点硬水与软水的区分,一定要加强记忆,综合应用.本考点主要出现在填空题和选择题中.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:推断题
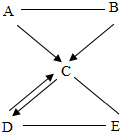 A、B、C、D、E都是初中化学的常见物质,它们存在如图所示的转化关系(“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系.部分反应物、生成物及反应条件已略去).其中A、B为单质且B是可供动植物呼吸的气体;D是一种盐,E是常用于改良酸性土壤的碱.请回答下列问题:
A、B、C、D、E都是初中化学的常见物质,它们存在如图所示的转化关系(“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系.部分反应物、生成物及反应条件已略去).其中A、B为单质且B是可供动植物呼吸的气体;D是一种盐,E是常用于改良酸性土壤的碱.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 汽油引起的火灾用水基型灭火器扑灭 | |
| B. | 用火碱溶液清洗餐具上的油污 | |
| C. | 井水浑浊时,向其中加明矾可以净水 | |
| D. | 洗发时,在用过洗发剂后再使用护发素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
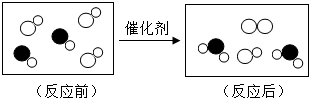 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法错误的是( )| A. | 参加反应的两种分子的个数比为1:1 | |
| B. | 原子在化学变化中是不可分的 | |
| C. | 图中共涉及四种物质 | |
| D. | 此反应可能为复分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
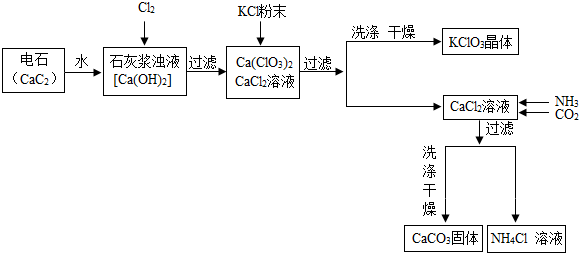
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com